Eine aktuellere Version dieses Artikels ist verfügbar, wurde aber noch nicht übersetzt.
Wir arbeiten an der Übersetzung des Artikels. Alternativ können Sie ihn in Englisch, Portugiesisch und Französisch lesen.
"Huntington’s Disease Therapeutics" Konferenz 2023 - Tag 3
Lesen Sie die neuesten Forschungsergebnisse von Tag 3 der "Huntington’s Disease Therapeutics" Konferenz 2023 #HDTC2023

 Von Joel Stanton, Dr Rachel Harding, Dr Leora Fox und Dr Tamara Maiuri 28. April 2023 Bearbeitet von Dr Sarah Hernandez Übersetzt von Michaela Winkelmann
Von Joel Stanton, Dr Rachel Harding, Dr Leora Fox und Dr Tamara Maiuri 28. April 2023 Bearbeitet von Dr Sarah Hernandez Übersetzt von Michaela Winkelmann
Willkommen zum dritten und letzten Tag der Huntington-Wissenschaft, live aus Dubrovnik, Kroatien!
Unsere Twitter-Updates sind unten zusammengestellt. Verfolgen Sie weiterhin die Live-Updates für den letzten Tag der Konferenz mit dem Hashtag #HDTC2023. Sehen Sie sich unsere Berichterstattung über Tag 1 hier an: https://de.hdbuzz.net/343 und über Tag 2 hier: https://de.hdbuzz.net/344.
Biomarker
Heute Morgen geht es um Biomarker, also Dinge, die wir messen können, um uns ein Bild von der Gesundheit einer Person oder ihrer Reaktion auf ein Medikament zu machen. Verschiedene Arten von Biomarker-Messungen können sich auf die Vorhersage des Krankheitsausbruchs, die Überwachung der HK einer Person oder die Überprüfung der Arzneimittelsicherheit konzentrieren. Wie wir gestern Abend gehört haben, kann der NfL-Spiegel uns helfen, ein besseres Bild von der Gesundheit des Gehirns zu bekommen, aber es gibt auch andere Proteine, die zu diesem Zweck untersucht werden.
HDClarity
Den Anfang macht Dr. Niels Henning Skotte von der Universität Kopenhagen, der uns über seine Arbeit zur Untersuchung von Biomarkern aus Proben von Huntington-Patienten berichten wird. Er verwendet Proben aus einer großen Studie zur Sammlung von Rückenmarksflüssigkeit namens HDClarity https://hdclarity.net/. Niels spricht zunächst über die Bedeutung der “Qualitätskontrolle” bei den Rückenmarksflüssigkeitsproben - Tests, mit denen sichergestellt wird, dass sie nicht kontaminiert und ordnungsgemäß gelagert sind. Er stellte auch einige Statistiken vor, um zu zeigen, wie viele Proben benötigt werden, um verschiedene Arten von Fragen zur HK zu beantworten. Viele der Proteine, die als Biomarker in Frage kommen, sind in den Patientenproben nur in winzigen Mengen vorhanden.
Es gibt spezielle Diagramme, so genannte “Vulkan-Plots”, mit denen die Forscher sehen können, welche Proteine in der Rückenmarksflüssigkeit von Menschen mit und ohne das HK-Gen am stärksten voneinander abweichen. Einige der potenziellen Biomarker zeigen sogar Unterschiede zwischen Gen-negativen und präsymptomatischen Genträgern, was bei der Suche nach Behandlungen hilfreich sein könnte, die vor dem Auftreten von Symptomen verabreicht werden können. Wenn sich bestimmte Proteinkonzentrationen im Blut und in der Rückenmarksflüssigkeit von Menschen mit und ohne Huntington unterscheiden, schauen sich die Forscher diese genauer an, um zu verstehen, wie und möglicherweise warum sich ihre Konzentrationen in verschiedenen Stadien der Huntington-Krankheit verändern. Wenn eine Proteinveränderung bei vielen Menschen gleich ist, kann sie als nützlicher Biomarker für die Huntington-Krankheit angesehen werden. Es wird untersucht, welche Rolle die verschiedenen Proteine im Körper spielen und wie sie miteinander interagieren, was uns Hinweise auf biologische Prozesse geben kann, die bei Huntington betroffen sind.
Im Zeitalter der künstlichen Intelligenz (KI) können Wissenschaftler große Datensätze in Computersysteme einspeisen und diese bitten, komplexe Faktoren zu berücksichtigen, um zu bestimmen, welche Proteine die besten Biomarker sind. Niels verwendet dazu Ansätze des maschinellen Lernens. In Zukunft könnte die Messung von Veränderungen in Gruppen von vielen Proteinen vor dem Auftreten von Symptomen dazu dienen, den genauen Verlauf der Krankheit zu verfolgen oder zu entscheiden, wann eine Huntington-Behandlung begonnen werden sollte.
Fettmoleküle als Biomarker für die HK
Der nächste Redner ist Dr. William Griffiths von der Universität Swansea, der uns darüber informieren wird, wie Cholesterin und andere Fettmoleküle als mögliche Biomarker für Huntington verwendet werden könnten. William erinnert uns daran, dass sich etwa 25 % des Cholesterins im Körper im Gehirn befinden, und ein Großteil davon wird vor Ort gebildet. Einige Cholesterinarten können das Gehirn verlassen, so dass wir in der Lage sein könnten, ihre Werte zu messen, um ein Verständnis für die Gesundheit des Gehirns zu gewinnen. Bei der Huntington-Krankheit wurde eine Störung des Cholesterinbildungsprozesses und eine Veränderung des Cholesterinspiegels beobachtet, und es gibt sogar Bestrebungen zur Entwicklung von Medikamenten, um diese Veränderungen zu korrigieren.
Williams Arbeit konzentriert sich auf die Messung der Unterschiede zwischen den Cholesterinwerten von Menschen mit und ohne Huntington, um herauszufinden, ob diese Moleküle als Biomarker verwendet werden können. Die Messung und Analyse von Cholesterin erfordert ausgeklügelte biochemische Techniken. Die spezifischen Moleküle, nach denen sie suchen, sind selbst mit den besten verfügbaren Geräten nur schwer nachzuweisen, so dass sie das System mit einer coolen Technik namens “Klick-Chemie” optimieren mussten. Dadurch wird das Signal des Cholesterins von der Größe eines Grases auf die Größe eines Baumes erhöht, wie William erklärt. Williams Gruppe hat herausgefunden, dass eine Form von Cholesterin, die nur in Neuronen gebildet wird, in Blutproben von Huntington-Patienten vermindert ist, was sie zu einem potenziellen Biomarker macht.
Somatische Instabilität als Biomarker für die HK
Nun wird Dr. Darren Monckton von der Universität Glasgow über die Forschungsarbeit seiner Gruppe berichten, die sich mit der Frage befasst, ob einige Aspekte der somatischen Instabilität ein Biomarker für Huntington sein könnten.
Wissenschaftler können den Grad der somatischen Instabilität des CAG-Repeat-Teils des HK-Gens in allen Arten von Patientenproben messen. Darren verwendet ausgeklügelte Sequenzierungstechniken, um dies so genau wie möglich an der DNA von Blutspenden von Menschen mit Huntington zu tun. Die Monckton-Gruppe hat kartiert, wie sich die Ausdehnung der CAG-Wiederholungen im Laufe der Zeit (somatische Instabilität) in Blutproben je nach Alter der Person und ihrer ursprünglichen CAG-Zahl unterschiedlich schnell verändert.
Sie haben auch Blutproben ein und derselben Person untersucht, die im Abstand von 7 Jahren entnommen wurden. Dies gibt Aufschluss darüber, wie die somatische Instabilität bei jeder Person im Laufe der Zeit zunimmt. Selbst in diesem riesigen Zeitrahmen sind die Veränderungen im Allgemeinen sehr subtil und vollziehen sich langsam. Die Möglichkeit, diese kleinen Veränderungen zu messen, ist sehr wichtig, da potenzielle Medikamente, die die Rate der somatischen Instabilität verändern, wahrscheinlich auch sehr subtile Auswirkungen haben werden.
Diese Techniken werden sich wahrscheinlich in einigen der geplanten klinischen Studien als sehr nützlich erweisen. Huntington ist nicht die einzige Krankheit mit somatischer Instabilität, und die vom Monckton-Labor entwickelten Techniken zur Messung subtiler DNA-Veränderungen im Laufe der Zeit werden sich auch für die Untersuchung anderer genetischer Krankheiten und entsprechender Behandlungen außerhalb von Huntington als nützlich erweisen.
Verfolgung von Huntington mit PET-Tracing
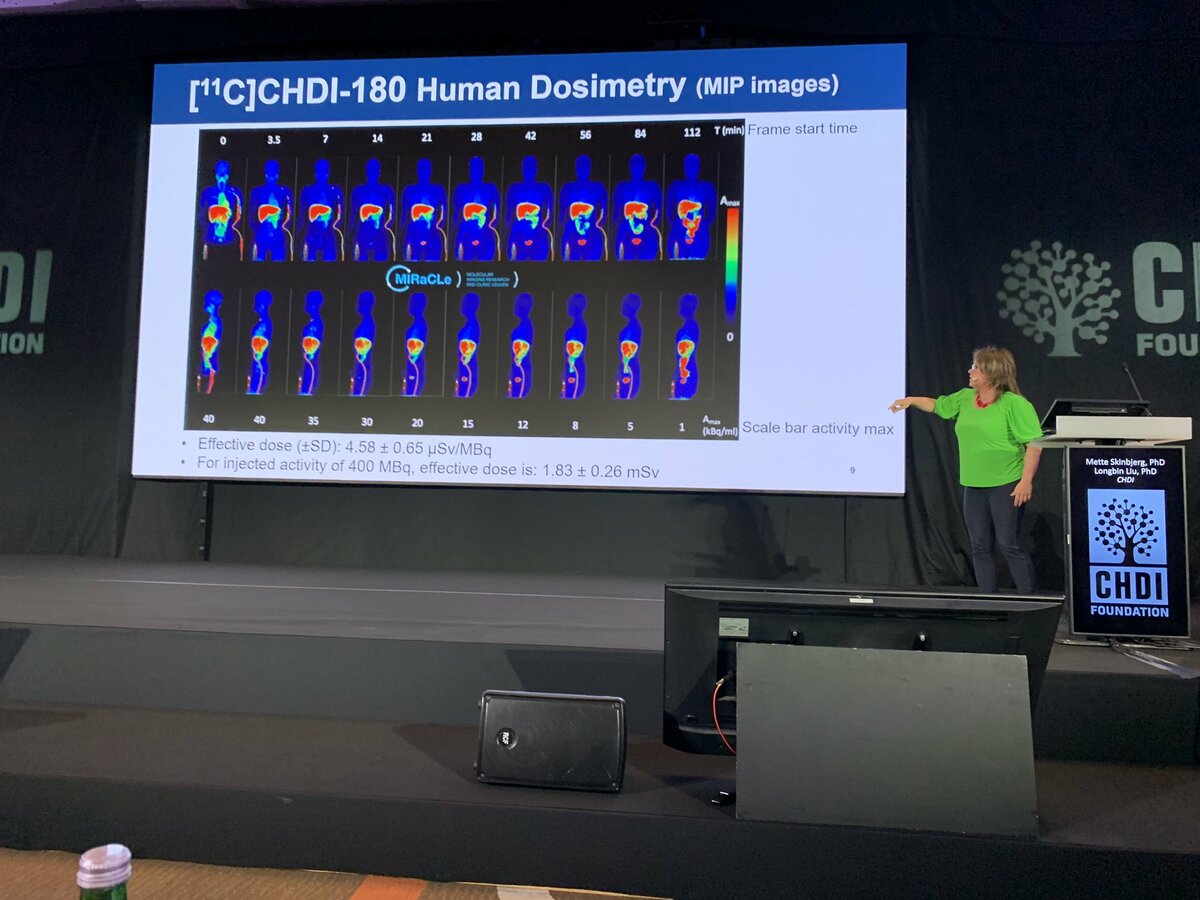
Nach der Kaffeepause berichtet Dr. Mette Skinbjerg über einen Huntingtin-PET-Tracer, mit dem sich die toxischen Eiweißklumpen im Gehirn, die sich im Laufe der Zeit ansammeln, aufspüren lassen. Wir haben bereits hier darüber geschrieben. Ohne einen Tracer können wir die Anhäufung des Huntingtin-Proteins im menschlichen Gehirn nur durch die Untersuchung von Proben nach dem Tod einer Person feststellen. Tracer sind ein sicherer Weg, um bei lebenden Menschen zu suchen, und könnten eine großartige Möglichkeit sein, um zu sehen, wie Medikamente wirken.
CHDI hat in Zusammenarbeit mit akademischen Partnern einen Tracer für die Huntington-Krankheit entwickelt, der in vielen verschiedenen Huntington-Tiermodellen, darunter Mäusen und Affen, eingehend charakterisiert wurde und es ermöglicht, den Aufbau von Proteinverklumpungen im Laufe der Zeit zu verfolgen. Jetzt gehen sie über die Tiermodelle hinaus und testen ihren Tracer an Menschen. Die Tracer sind mit Radioaktivität markiert, so dass die Wissenschaftler messen können, wo sie am Ziel haften - in diesem Fall an den Klumpen. Es ist wichtig, dass die Tracer den Körper nach der Verabreichung verlassen, damit die Radioaktivität im sicheren Bereich bleibt.
Obwohl der Tracer bei Menschen sicher zu sein scheint, entsprach das Signal im Gehirn leider nicht dem, was die Wissenschaftler erwartet hatten. Das ist enttäuschend, aber dieses Programm hat uns viel über die Herstellung eines Tracers für Huntington gelehrt, der in Zukunft für die Entwicklung besserer Tracer verwendet werden kann. Jetzt arbeitet das Team an einer neuen Generation von Tracern, von denen es hofft, dass sie viel besser funktionieren. Die Arbeiten im Labor schreiten voran, und es werden zahlreiche Tests an Huntington-Tieren durchgeführt, so dass die nächste Runde hoffentlich besser verläuft.
Biomarker und maschinelles Lernen
Der nächste Redner ist Dr. Peter Wijeratne von der University of Sussex. Seine Gruppe will Biomarker und maschinelles Lernen einsetzen, um das Fortschreiten der Huntington-Krankheit bei Einzelpersonen zu charakterisieren und vorherzusagen. Sehr cool!
Da die Forscher weiterhin alle Arten von Biomarkern aus Bioflüssigkeiten, bildgebenden Verfahren usw. identifizieren, könnten viele Biomarker für eine Person kombiniert werden, um bessere Vorhersagen zu treffen. Aber all diese Daten miteinander zu kombinieren und zu verstehen, ist für den Menschen schwer zu bewerkstelligen.
Peter erläuterte anhand eines lustigen ChatGPT-Beispiels das maschinelle Lernen - ein Algorithmus, der sich anpassen und aus Datenmustern Schlüsse ziehen kann. Er zeigte, wie schnell diese Systeme neue Informationen lernen und fundierte Entscheidungen treffen können - sehr cool! Um das KI-System zu “trainieren”, braucht man viele, viele hochwertige Trainingsdaten, bei denen die Wissenschaftler die Antworten bereits kennen. Das KI-System kann dann lernen, Muster in diesen Daten zu erkennen, wodurch es in der Lage ist, ähnliche und verwandte Muster in Testdaten zu erkennen, bei denen die Antworten noch nicht bekannt sind.
Peters Gruppe untersucht die Bildgebungsdaten des Gehirns aus drei verschiedenen Studien, in denen untersucht wurde, wie sich verschiedene Gehirnstrukturen bei Huntington im Laufe der Zeit verändern. Durch das Training von KI auf diesen komplexen und umfangreichen Datensätzen hoffen sie, robuste Vorhersagen über die Krankheit treffen zu können. Wie sich herausstellte, konnten gute Vorhersagen für den Ausbruch der Krankheit gemacht werden, und die Ergebnisse stimmten gut mit dem HD-ISS-Staging-System überein. Die Forscher hoffen, dass sich dies in Zukunft als nützlich erweisen wird, um Vorhersagen auf individueller Ebene zu treffen.
HTT-Spiegel und Tominersen
Im nächsten Vortrag wird Dr. Blair Leavitt, ein Kliniker/Forscher von der University of British Columbia, über seine Studie mit Proben aus der GENERATION HD1-Studie mit Tominersen sprechen. Er geht der Frage nach, wie sich der Huntingtin-Spiegel unter der Behandlung mit Tominersen verändert.
Blair beginnt mit einem Dank an die HK-Familienmitglieder, die so großzügig und selbstlos biologische Proben mit Wissenschaftlern teilen, um eine Biobank-Ressource zu schaffen. Dies ist für die Wissenschaftler von unschätzbarem Wert, um die Huntington-Krankheit zu verstehen und herauszufinden, wie Medikamente den Verlauf dieser Krankheit verändern können. Blair konzentriert sich insbesondere auf eine Person, der es ein Anliegen war, sein Gehirn zu spenden, als er starb. Aus den Tominersen-Studien, an denen er teilgenommen hat, stehen zahlreiche Daten und Proben zur Verfügung, ebenso wie sein Hirngewebe, das einen seltenen Einblick in die Auswirkungen von Medikamenten bietet.
Bei der Untersuchung des Gehirns konnten die Wissenschaftler von Blairs Team die Konzentration des Medikaments in verschiedenen Regionen messen und mit den in früheren Affenversuchen vorhergesagten Expositionswerten vergleichen. Dabei zeigte sich, dass die Vorhersagen im Allgemeinen recht gut waren. Als Nächstes untersuchten sie die Huntingtin-Konzentrationen in verschiedenen Hirnregionen und verglichen diese mit denen von Kontrollgehirnen. Wie bei einer Huntingtin-senkenden Behandlung zu erwarten, waren die Werte bei diesen Personen viel niedriger als bei den Kontrollpersonen. Enttäuschend ist, dass die Huntingtin-Konzentrationen in der Rückenmarksflüssigkeit zu niedrig waren, um bei dieser Person quantifiziert werden zu können. Das bedeutet, dass wir nicht wissen, wie gut die Huntingtin-Werte im Gehirn und in der Rückenmarksflüssigkeit korrelieren, zumindest bei diesem Studienteilnehmer.
Man kann gar nicht hoch genug einschätzen, wie wertvoll dieses Gewebe für die Wissenschaftler ist, um wirklich eingehend untersuchen zu können, wie sich eine Behandlung auf das Gehirn ausgewirkt hat. Die Mitarbeiter im Publikum werden anhand des von diesem Studienteilnehmer so großzügig gespendeten Gewebes weitere Fragen stellen.
Klinische Studien
Nach einer Mittagspause geht es weiter mit der letzten wissenschaftlichen Sitzung der #HDTC2023-Konferenz. Die Sitzung am Nachmittag wird sich auf klinische Studien konzentrieren, und wir werden über Studiendesign und Fortschritte in der Humanforschung hören.
Klassifizierung von HK-Stadien
Dr. Jeff Long von der University of Iowa spricht über das HD-ISS, ein Klassifizierungssystem für die HK. Dabei handelt es sich um ein Instrument für die klinische Forschung, das es den Forschern ermöglicht, Menschen in den frühen Stadien der Huntington-Krankheit besser zu klassifizieren, um Studien effizienter zu gestalten und Patienten zu rekrutieren.
Jetzt, da dieses neue Instrument breiter eingesetzt wird, entwickelt Jeffs Team eine Datenbank mit Informationen aus großen Beobachtungsstudien wie IMAGE-HD, PREDICT-HD, TRACK-HD und ENROLL-HD, um den zeitlichen Verlauf des Fortschreitens der HD-ISS-Stadien besser zu verstehen. Nachdem Jeffs Team diese Instrumente entwickelt hat, arbeitet es daran zu verstehen, wie sie in einer klinischen Studie nützlich sein könnten - wie viele HK-Patienten in einem bestimmten Krankheitsstadium wären nötig, um zuverlässige Ergebnisse zu erhalten, die uns davon überzeugen, ob ein Medikament wirkt oder nicht.
Da das HD-ISS Daten aus Hirnbildern, Biomarkern und Genetik umfasst, können viele Variablen berücksichtigt werden, um zu definieren, welche klinischen Messungen am besten geeignet sind, um zu zeigen, ob ein neues Medikament wirkt. Mithilfe von Datenbanken mit Beobachtungsstudien können Forscher wie Jeff statistische Verfahren anwenden, um besser vorauszusagen, wie viele Teilnehmer und welche Arten von Bewertungen wahrscheinlich erforderlich sind, um den Nutzen eines Medikaments nachzuweisen. Dies ist eine komplexe und wichtige Mathematik, die zeigt, wie wichtig die Teilnahme an Beobachtungsstudien ist.
Der Beweis liegt im Pudding (oder in den Daten)
Der nächste Vortrag wird mit Spannung erwartet, denn es geht um die ersten Ergebnisse der PROOF-HD-Studie zu Pridopidin. Aus der Presse haben wir am Dienstag erfahren, dass die Studie ihre primären Endpunkte nicht erreicht hat, aber jetzt sehen wir die Daten.
Dr. Michael Hayden, der CEO von Prilenia, hält diesen Vortrag. Er erklärt zunächst den Mechanismus, wie das Medikament vermutlich auf Nervenzellen wirkt, insbesondere seine Wirkung auf einen Rezeptortyp, der die Kommunikation zwischen Neuronen erleichtert, bekannt als Sigma 1.
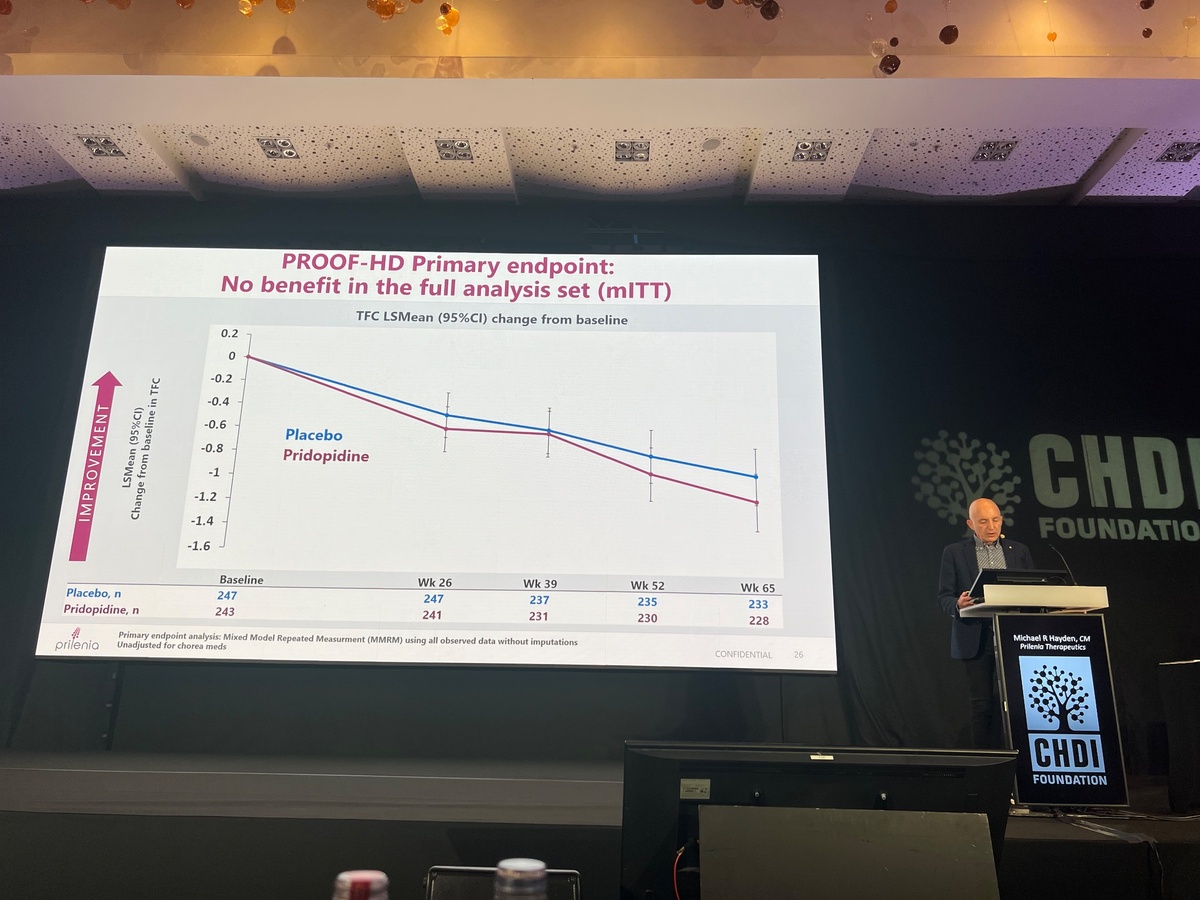
Die PROOF-HD-Studie war darauf ausgelegt, anhand bestimmter klinischer Bewertungen, einer Kombination aus Bewegungs-, Verhaltens- und Denktests, festzustellen, ob Pridopidin dazu beiträgt, die Verschlechterung der Huntington-Symptome über einen Zeitraum von etwa anderthalb Jahren zu verlangsamen. Studien werden mit “primären”, “sekundären” und “explorativen” Endpunkten konzipiert. Der Nachweis, dass ein Medikament die primären Endpunkte beeinflusst, ist in der Regel ausschlaggebend für die Entscheidung, das Medikament weiter zu entwickeln und schließlich zuzulassen. Diese Studie wurde schnell rekrutiert, und die meisten Teilnehmer blieben die ganze Zeit über dabei - ein Beweis für die Mobilisierung und das Engagement der HK-Patienten. Wenn die überwiegende Mehrheit der Teilnehmer an einer langen Studie teilnimmt, kann dies auch ein Hinweis auf die Sicherheit und Verträglichkeit des Medikaments sein.
Das wichtigste Gesamtergebnis ist, dass die primären Endpunkte der Studie nicht erreicht wurden. In diesem Fall handelte es sich um eine Messung der Fähigkeit der Teilnehmer, im Alltag zurechtzukommen. Im Durchschnitt funktionierten Pridopidin- und Placebo-Patienten während der gesamten Studiendauer ähnlich gut. Ein weiterer wichtiger Endpunkt war eine Kombination aus verschiedenen Bewegungs-, Verhaltens- und Denkmessungen, die sich bei den Pridopidin-Teilnehmern ebenfalls nicht verbesserten. Pridopidin könnte sich bei einer Bewegungsmessung, dem sogenannten Q-Motor, als vorteilhaft erwiesen haben, doch war dies statistisch nicht signifikant.
Wenn eine Studie konzipiert ist, aber bevor sie beginnt, muss der Sponsor (in diesem Fall Prilenia) Entscheidungen darüber treffen, welche Arten von Statistiken und Analysen er nach Vorliegen der Ergebnisse durchführen wird. In der PROOF-HD-Studie entschied Prilenia, die Teilnehmer in Gruppen aufzuteilen, die Medikamente, sogenannte Neuroleptika (auch als Neuropsychotika bekannt), einnehmen, und solche, die keine Neuroleptika einnehmen. Der Grund dafür ist, dass Pridopidin einige der gleichen biologischen Signalwege beeinflusst wie Neuroleptika. Als Prilenia nur die Daten von Personen untersuchte, die keine Neuroleptika einnahmen, war der potenzielle Nutzen anhand einiger klinischer Messungen deutlicher, insbesondere im ersten Jahr. Letztlich war aber auch dies statistisch nicht signifikant.
Michael zeigt nun Daten aus einer Studie mit Pridopidin bei Menschen mit ALS, einer Krankheit, die einige biologische Gemeinsamkeiten mit der Huntington-Krankheit aufweist. Auch diese Studie zeigte einige potenzielle Vorteile bei sekundären Endpunkten.
Prilenia ist der Ansicht, dass Pridopidin für die Behandlung der Huntington-Krankheit vielversprechend ist, und das Unternehmen wird sich nun darauf konzentrieren, die Daten genauer zu untersuchen. Das Unternehmen wird sich nun darauf konzentrieren, die Daten zu vertiefen, insbesondere um zu verstehen, wie verschiedene Neuroleptika-Behandlungen das Ansprechen auf das Medikament beeinflussen.
Rotes Licht für Branaplam
Als Nächstes beschreibt Dr. Beth Borowsky von Novartis die Ergebnisse ihrer Studie mit einem Medikament namens Branaplam bei Patienten mit Huntington-Erkrankung. Über dieses Medikament und seinen überraschenden Wirkmechanismus haben wir hier geschrieben.
Während sich Branaplam bei Kindern mit einer anderen Krankheit (spinaler Muskelatrophie) als sicher erwies, deuteten einige Tierversuche auf die Möglichkeit einer Schädigung der Nerven hin, die vom Gehirn zur Haut und zu den Muskeln des Körpers führen. Aufgrund dieser Bedenken nahm Novartis unter den behandelten Huntington-Patienten auch Experten für diese Art von Nervenschäden auf, nur für den Fall, dass ein solches Symptom während der Studie auftritt.
Leider deuteten im Laufe einiger Wochen einige subtile Bewegungen und Labormessungen darauf hin, dass die befürchteten Risiken tatsächlich aufgetreten waren. In Absprache mit ihren unabhängigen Sicherheitsexperten beschloss Novartis, die Dosierung zunächst zu unterbrechen. Zum Zeitpunkt der Unterbrechung hatten die Patienten eine Behandlung zwischen 5 und 22 Wochen erhalten. Nach sorgfältiger Prüfung wurde festgestellt, dass 78 % der behandelten Patienten ein oder mehrere Anzeichen aufwiesen, die auf eine Nervenschädigung hindeuten könnten, sowie einige Veränderungen in den Gehirnstrukturen, den sogenannten Ventrikeln.
Auf der Grundlage einer sehr sorgfältigen Analyse des Nutzens und der Risiken für die Patienten beschloss Novartis, die Studie im Dezember 2022 abzubrechen. Wir haben hier darüber berichtet. Derzeit werden alle Studienteilnehmer weiterhin auf Symptome von Nervenschäden überwacht und es wird beobachtet, wie sich diese im Laufe der Zeit verändern, nachdem sie das Medikament abgesetzt haben.
Beth hat eine Momentaufnahme der von Novartis gesammelten Daten vorgelegt, um die Huntington-Gemeinschaft auf den neuesten Stand zu bringen, was sie herausgefunden haben. Erstens: Wie erhofft, senkte Branaplam den Huntingtin-Spiegel in der Rückenmarksflüssigkeit um etwa 25 %, was darauf hindeutet, dass Branaplam den Huntingtin-Spiegel im Gehirn senken konnte.
Leider fand Novartis auch höhere Werte eines Proteins namens Neurofilament Light (NfL), eines Markers für unglückliche Gehirnzellen. Wir haben bereits früher über NfL gesprochen, da es im normalen Verlauf der Huntington-Krankheit ansteigt, und es war ein wichtiger Schwerpunkt der Sitzung über Biomarker auf dieser Tagung. Wir hoffen, dass die NfL-Werte im Laufe der Zeit sinken, wenn ein HK-Medikament wirkt. In der Branaplam-Studie entdeckte Novartis jedoch, dass der NfL-Spiegel im Blut und in der Rückenmarksflüssigkeit unter der Behandlung anstieg. Dies ist einer der Befunde, die Novartis dazu veranlassten, die Studie zu unterbrechen.
Parallel zu diesen Labortests führten die Ärzte bei jedem Teilnehmer sorgfältige Untersuchungen der Nervenfunktionen durch. Etwa 86 % der Teilnehmer hatten irgendeine Art von neurologischen Symptomen, und die Bildgebung des Gehirns zeigte größere, mit Flüssigkeit gefüllte Hohlräume, die so genannten Seitenventrikel.
Alles in allem scheint das Medikament von Novartis genau das zu bewirken, was man sich erhofft hatte - eine Verringerung der Huntingtin-Konzentration im Gehirn. Leider ging dies mit schwerwiegenden Nebenwirkungen einher, so dass es für dieses Medikament keinen sicheren Weg in die Zukunft gibt. Wichtig ist, dass Novartis die Studienteilnehmer weiterhin beobachtet und die Daten analysiert, um die weitere Entwicklung des Medikaments zu unterstützen.
AMT-130 schreitet voran
Als Nächstes berichtet Dr. Talaha Ali von uniQure über den neuesten Stand ihrer Studie zu einer Gentherapie für die HK namens AMT-130. Diese beruht auf der Injektion harmloser Viren, die Anweisungen enthalten, die den Gehirnzellen beibringen, wie sie die HTT-Werte senken können.
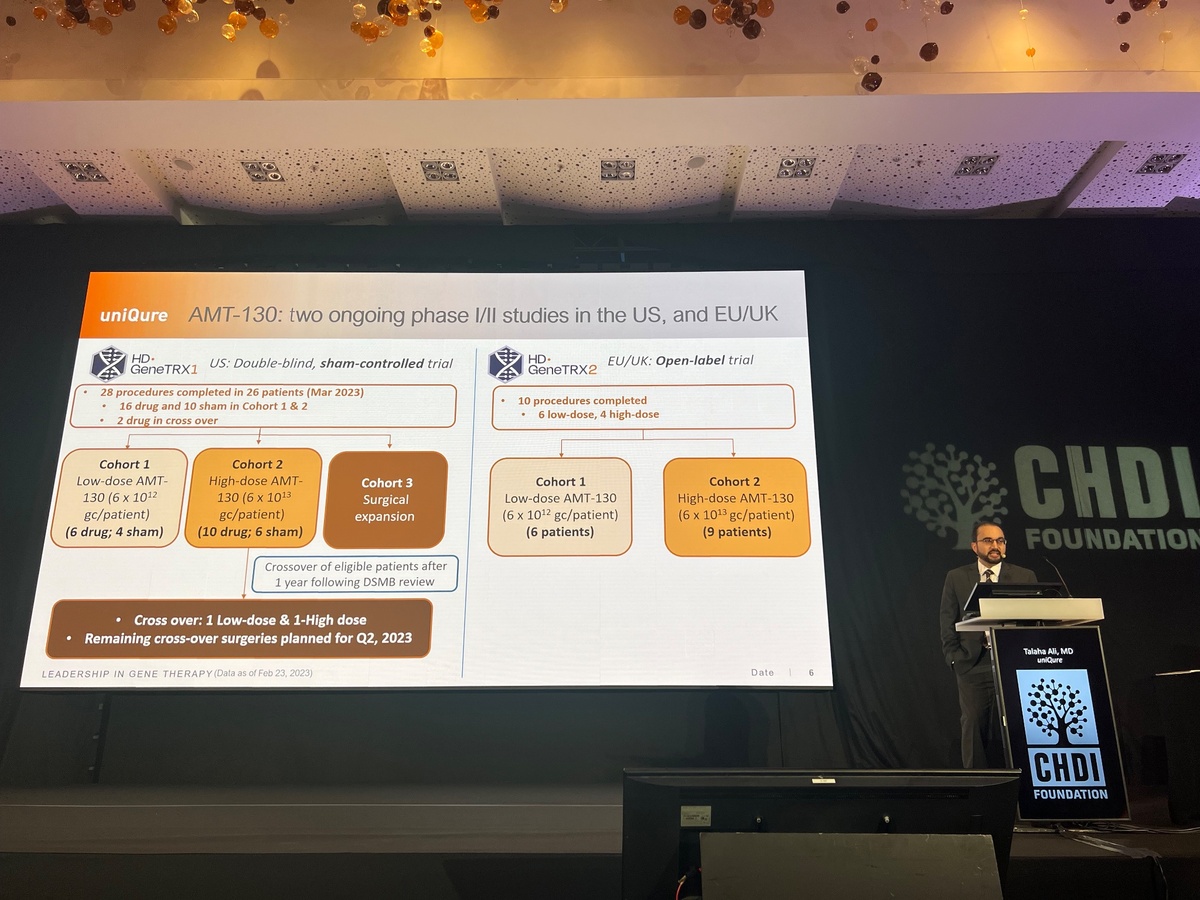
Das Erstaunliche an diesen viralen Gentherapien ist, dass sie theoretisch nur eine einzige Injektion erfordern, da die Viren viele Jahre lang - vielleicht für immer - im Gehirn verbleiben. Der Nachteil ist, dass ein chirurgischer Eingriff erforderlich ist, um die Viren in das Gehirn einzubringen. Dieser chirurgische Ansatz wird derzeit in zwei getrennten Studien getestet - eine in den USA und eine in Europa. Da es sich hierbei um ein hochmodernes Verfahren handelt, wird nur eine kleine Anzahl von Patienten in die Studie aufgenommen - insgesamt etwa 40 Patienten.
Die an der Studie teilnehmenden Patienten erhalten eine sehr vorsichtige, sehr langsame Injektion des Medikaments in verschiedene Teile der tiefen Hirnstrukturen, die bei Huntington am stärksten betroffen sind. Im Rahmen der Studie werden eine niedrige und eine hohe Dosis von AMT-130 getestet und die Teilnehmer im ersten Jahr und dann bis zu fünf Jahre lang in kürzeren Abständen überwacht. uniQure wird in Kürze, voraussichtlich Ende Juni 2023, neue Daten und Aktualisierungen veröffentlichen.
Wie bereits berichtet, hatte uniQure im Laufe der Studie einige besorgniserregende Reaktionen bei drei Patienten. Nach sorgfältiger Prüfung entschieden die unabhängigen Ärzte, die diese Symptome überwachten, dass das Risiko akzeptabel erschien, und die Studie wurde fortgesetzt.
Erfreulicherweise hat uniQure einige Hinweise darauf, dass AMT-130 die Huntingtin-Konzentration im Liquor verringert - allerdings ist die Zahl der behandelten Patienten bisher viel zu gering, um genaue Schätzungen vornehmen zu können. Das nächste Mal, wenn wir von uniQure hören, werden wir hoffentlich mehr interessante Daten erhalten!
Einschränkung der Ziele für Tominersen
Der nächste Vortrag wird von Dr. Peter McColgan von Roche gehalten, das ein Medikament namens Tominersen für die HK entwickelt. Er wird über die Geschichte des Programms sprechen, über die Erkenntnisse aus den Tominersen-Studien und über die laufende GENERATION HD2-Studie.
Ionis hat ursprünglich Tominersen entwickelt, ein genetisches Medikament, das über das Rückenmark verabreicht wird und als ASO bezeichnet wird. In frühen, kurzen Sicherheitsstudien war es das erste Medikament, das den Huntingtin-Spiegel beim Menschen senken konnte. Es folgte eine sehr große Studie zur Untersuchung der Auswirkungen auf die Symptome der Huntington-Krankheit, bekannt als GENERATION HD1. Im März 2021 erfuhren wir, dass GENERATION HD1 wegen Sicherheitsbedenken gestoppt wurde - Tominersen half den Huntington-Patienten nicht, und in der höchsten Dosis könnte es sogar schaden.
Später untersuchte Roche die Daten genauer und stellte fest, dass einige Teilnehmer an GENERATION HD1 möglicherweise von Tominersen profitierten, insbesondere diejenigen, die die Studie in einem jüngeren Alter und mit weniger schweren Symptomen begannen. Aus diesem Grund hat Roche die GENERATION HD2-Studie konzipiert und gestartet. Dabei handelt es sich um eine kleinere Studie, in der Tominersen bei einer jüngeren Population von Menschen im frühesten Stadium der HK getestet wird. Die Rekrutierung für diese Studie läuft bereits, und es werden bis zu 75 Standorte in 15 Ländern beteiligt sein.
Peter zeigt nun Daten zu NfL, einem Protein, das als Marker für die Schädigung von Nervenzellen dienen kann. Neue Analysen von Daten aus GENERATION HD1 zeigen, dass die Verabreichung von Tominersen in niedrigeren Dosen wahrscheinlich sicherer ist, da die NfL-Werte niedriger sind. In der GENERATION HD2-Studie werden zwei verschiedene, niedrigere Tominersen-Dosen getestet, und die mathematische Modellierung sagt voraus, dass diese niedrigeren Dosen sicherer sind, weil sie nicht zu einem so starken Anstieg der NfL führen.
Jetzt stellt Peter neue NfL-Daten aus der GENERATION HD1-Studie vor. Gegen Ende der Studie sieht es tatsächlich so aus, als ob die NfL-Werte unter Tominersen sinken, was ein weiterer Beweis dafür ist, dass die niedrigeren Dosen, die in GENERATION HD2 getestet werden, vielversprechend sein könnten.
Hier finden Sie Peters gesamte Präsentation zu Tominersen.
Damit sind die Forschungsvorträge auf der HD Therapeutics Conference 2023 abgeschlossen. Vielen Dank, dass Sie uns gefolgt sind, und besuchen Sie http://hdbuzz.net, um die Zusammenfassungen von Tag 1, Tag 2 und Tag 3 zu lesen!


