Details zur ersten klinischen Studie zur Gentherapie bei Huntington-Krankheit werden bekannt
UniQure gibt wichtige Details seiner geplanten Studie zur Bewertung der Sicherheit und Fähigkeit der AMT-130-Gentherapie zur Senkung des problematischen Huntingtin-Proteins mithilfe eines „Single-Shot“-Virus-Verabreichungssystems bekannt.
Auf der jüngsten Jahrestagung der Huntington’s Disease Society of America in Boston gab UniQure wichtige Details zu seiner geplanten klinischen Studie für seine experimentelle Therapie AMT-130 bekannt. Wir haben zuvor hier über AMT-130 geschrieben, daher behandelt dieser Artikel die Grundlagen und das, was gerade angekündigt wurde.
Huntingtin-senkende Gentherapie in Kürze
AMT-130 ist eine Huntingtin-senkende Behandlung, da es versucht, die Produktion des schädlichen mutierten Huntingtin-Proteins zu reduzieren, das für Neuronen schädlich ist und die Ursache der Huntington-Krankheit ist.

AMT-130 unterscheidet sich jedoch in einigen wichtigen Punkten von den Anti-Sense-Oligonukleotid (ASO)-Studien, die derzeit von Roche und Wave Life Sciences durchgeführt werden.
AMT-130 ist eine Gentherapie, was bedeutet, dass es versucht, die genetische Ausstattung des behandelten Patienten dauerhaft zu verändern. AMT130 versucht nicht, die HD-Mutation zu löschen – das ist viel schwieriger zu erreichen, als man denkt. Stattdessen verwendet AMT130 ein harmloses Virus, das als Adeno-assoziiertes Virus (AAV) bekannt ist, um den Neuronen ein kleines zusätzliches Stück genetischen Code
Sobald ein Neuron mit AMT-130 behandelt wurde, produziert es kontinuierlich zusätzliche Kopien des neuen Huntingtin-senkenden Moleküls. Obwohl das Neuron immer noch das schädliche HD-Gen enthält und immer noch Botschaften zur Herstellung des mutierten Huntingtin-Proteins sendet, produziert es gleichzeitig eine neue Reihe von Anweisungen, um die Huntingtin-Botschaft zu löschen. Das Ergebnis sollte eine reduzierte Produktion des schädlichen Proteins sein, mit einer sehr langen Wirkdauer – möglicherweise lebenslang.
Was ist mit der Studie?
UniQure hat einige vorläufige, aber wichtige Details über seine geplante Studie in einer Erklärung an die HD-Community bekannt gegeben. Hier ist, was wir bisher wissen.
Der Schwerpunkt der ersten Studie wird auf Sicherheit und Verträglichkeit liegen – herauszufinden, ob es schädliche oder unangenehme Auswirkungen der Behandlung mit AMT-130 gibt.
UniQure schließt auch die Wirksamkeit in die erklärten Ziele der Studie ein: Das bedeutet, eine Vorstellung davon zu bekommen, ob die Behandlung das tut, was sie soll. Im weiteren Sinne bedeutet das, das Fortschreiten der Huntington-Krankheit zu verlangsamen. Es ist theoretisch möglich, aber sehr unwahrscheinlich, dass diese kleine erste Studie Beweise für ein verlangsamtes Fortschreiten zeigen wird. Ein erreichbareres Ziel ist es, zu testen, ob die Behandlung die Huntingtin-Produktion reduziert, was wir jetzt mit Techniken messen können, die wir auf HDBuzz hier beschrieben haben.
Die AMT-130-Studie wird an HD-Kliniken in den Vereinigten Staaten durchgeführt. Wir wissen noch nicht, welche Standorte oder wie viele. Diese werden öffentlich bekannt gegeben, sobald sie online sind. UniQure hofft, vor Ende 2019 mit der Aufnahme von Patienten beginnen zu können.
An der Studie werden nur 26 Patienten mit frühen Symptomen der Huntington-Krankheit teilnehmen. Das bedeutet Menschen mit abnormalen Bewegungen, innerhalb der ersten Jahre, nachdem die Diagnose von einem Neurologen „offiziell“ bestätigt wurde. Die Altersspanne beträgt 25 bis 65 Jahre.
Ungewöhnlicherweise hat uniQure einen Grenzwert von 44 CAG-Wiederholungen oder mehr im HD-Gen festgelegt. Etwa 50 % der Menschen mit einem positiven Gentest für HD haben zwischen 40 und 45 Wiederholungen, so dass dieser Grenzwert wahrscheinlich einige Leute ausschließen wird. Es ist wahrscheinlich, dass uniQure diesen Grenzwert festgelegt hat, um die Studie auf Personen auszurichten, die wahrscheinlich schneller fortschreiten, so dass sie eine bessere Chance haben, zu zeigen, dass AMT-130 das Fortschreiten verlangsamt.
Die 26 Patienten werden nach dem Zufallsprinzip in zwei Gruppen aufgeteilt. 16 Patienten erhalten eine aktive Behandlung mit AMT-130, entweder in einer niedrigen oder einer hohen Dosis. 10 Patienten unterziehen sich einer „Nachahmungs“-Behandlung, die auch als „Placebo“- oder „Schein“-Behandlung bezeichnet werden könnte.
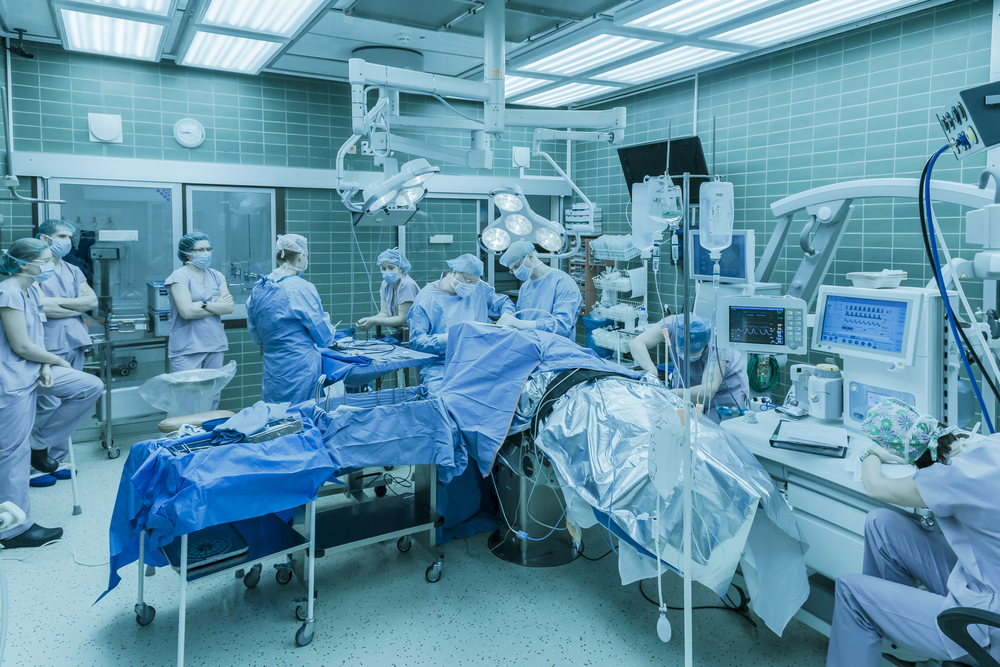
Der potenziell große Vorteil der Behandlung mit AMT-130 ist, dass sie nur einmal pro Teilnehmer durchgeführt wird, aber es ist eine große Sache. Sie beinhaltet eine Gehirnoperation, die unter Vollnarkose durchgeführt wird. Zwischen zwei und sechs kleine Löcher werden in den Schädel gebohrt, und dünne Schläuche, sogenannte Katheter, werden in das Gehirn eingeführt. Der AMT-130-Cocktail wird dann durch die Schläuche in das Gehirn injiziert.
Patienten, die der Nachahmungsbehandlung zugeteilt wurden, werden sich einer Vollnarkose unterziehen, und es werden flache Löcher in die äußere Schicht des Schädels gebohrt, die aber nicht ganz durch ihn hindurchgehen. Es sind keine Schläuche oder Injektionen beteiligt.
Der Zweck der Nachahmungsgruppe ist es, herauszufinden, ob irgendwelche Effekte, die in der Studie beobachtet werden – seien sie hilfreich oder schädlich – durch die AMT-130-Therapie selbst, den Placebo-Effekt (der psychologische Schub, der von der Teilnahme an einer klinischen Studie kommt) oder die Auswirkungen der Narkose und Operation verursacht werden.
Die Patienten werden 18 Monate lang intensiv nachbeobachtet, mit Untersuchungen wie MRT-Scans und Lumbalpunktionen (Spinal Taps). Patienten in der aktiven Gruppe werden dann gebeten, 5 Jahre lang zu jährlichen Besuchen wiederzukommen.
Das neurochirurgische Team wird wissen, welche Patienten sich in welcher Gruppe befinden, aber der Patient und das HD-Studienteam werden es nicht wissen. Das bedeutet, dass die Studie doppelblind ist und hilft, den Placebo-Effekt zu minimieren, so dass die Studie ihr wissenschaftliches Ziel erreichen kann, herauszufinden, ob das Medikament sicher ist und ob es wirkt.
Der Vorteil für Patienten, die der Nachahmungsgruppe zugeteilt wurden, ist, dass sie 18 Monate nach ihrer Mini-Operation, wenn eine unabhängige Überprüfung der Studiendaten zufriedenstellend ist, eingeladen werden, sich einer vollständigen Behandlung mit AMT-130 in einer zweiten, größeren Operation zu unterziehen.
Risiko und Belohnung
Der größte potenzielle Vorteil von AMT-130 ist auch sein größter potenzieller Nachteil. Es ist eine Gentherapie, so dass eine einmalige Behandlung voraussichtlich dauerhaft sein wird.
Wenn alles wie geplant verläuft, wird es eine Behandlung sein, die früh nach einem positiven Gentest-Ergebnis gegeben werden könnte, die lang anhaltende, möglicherweise lebenslange Vorteile hat. Sie könnte das Fortschreiten verlangsamen oder sogar den Ausbruch von HD verzögern, ohne dass wiederholte Dosierungen erforderlich sind.
Wenn sich die Behandlung jedoch als schädliche Nebenwirkungen herausstellt, könnten diese auch lange anhalten – und es gibt keine Möglichkeit, die Behandlung abzuschalten, sobald sie gegeben wurde. Als rein fiktives Beispiel: Was wäre, wenn die Behandlung aus irgendeinem Grund eine Verschlechterung der Bewegungskontrolle, eine Beschleunigung der Huntington-Krankheit der Person oder ein permanentes Gefühl von Übelkeit verursacht? Patienten könnten mit schweren Symptomen oder sogar Behinderungen zurückgelassen werden. Das medizinische Team würde alles tun, was es kann, um die Dinge zu verbessern, aber das Entfernen der Behandlung oder das Abschalten wird keine Option sein.
Ein weiteres wichtiges Detail ist, dass AMT-130 entwickelt wurde, um die Produktion beider Formen des Huntingtin-Proteins zu reduzieren – nicht nur die schädliche mutierte Form, sondern auch ihr unschuldiges „normales“ Geschwisterchen, das Wissenschaftler „Wildtyp“ nennen. Eine Sorge ist, dass die Reduzierung von Wildtyp-Huntingtin im Gehirn von Erwachsenen mit HD mit eigenen Risiken verbunden sein könnte, die alle Vorteile der Senkung des mutierten Proteins in den Schatten stellen könnten. Diese Bedenken stammen größtenteils aus Experimenten, die an Mäusen durchgeführt wurden, die alle große Unterschiede zu menschlichen Patienten aufweisen, und im Moment sind die tatsächlichen Auswirkungen der Senkung von Wildtyp-Huntingtin bei Patienten unbekannt. Wichtige Erkenntnisse hierzu werden hoffentlich aus den beiden laufenden Huntingtin-senkenden Programmen gewonnen, bei denen Medikamente in die Wirbelsäule injiziert werden: Roches RG6042, das beide Formen des Proteins senkt, und Waves Precision-HD-Programm, das versucht, die mutierte Form selektiv zu senken.
AMT-130 wurde an Tieren getestet und wäre nicht zu einer Humanstudie zugelassen worden, wenn inakzeptable Risiken entdeckt worden wären. Aber nur Menschen können uns sagen, welche Vorteile und Schäden zu erwarten sind. Zusätzlich zu den Risiken der Operation können Patienten, die eine Teilnahme an dieser Studie in Erwägung ziehen, erwarten, dass sie gründlich über die möglichen Risiken beraten werden, ohne dass eine feste Erwartung besteht, dass sie persönlich von der Teilnahme profitieren werden. Solche Freiwilligen werden gebeten, im Namen anderer erhebliche Opfer zu bringen – diejenigen, die sich für First-in-Human-Studien melden, gehören zu den größten individuellen Helden der HD-Community.
Ein wichtiger Fortschritt
Hier bei HDBuzz heißt unser Lieblingscocktail Substantielle Hoffnung. Er besteht zu gleichen Teilen aus Optimismus und Realismus. Nach unserer vorherigen Berichterstattung über Huntingtin-senkende Therapien haben wir einige Rückmeldungen erhalten, dass wir zu positiv sind, und einige, dass wir zu negativ sind (das Wort „HDBuzzKill“ wurde sogar herumgereicht, und wir sind damit einverstanden). Vielleicht bedeutet das, dass wir es ungefähr richtig machen – aber es liegt an Ihnen, zu entscheiden.
Wir ermutigen alle Leser, ihre Informationen aus mehreren Quellen zu beziehen. Unser ‚Zehn Goldene Regeln‘-Artikel, der 2011 veröffentlicht wurde, könnte Ihnen helfen, einen Geist zu entwickeln, der offen für coole neue Ideen ist, aber gesund skeptisch gegenüber Hype ist. Wir befürworten uneingeschränkt, dass HD-Familienmitglieder sich freiwillig für Forschungsprojekte einschließlich klinischer Studien melden: Dies ist der einzige Weg, wie wir jemals echte Fortschritte im Kampf gegen die Huntington-Krankheit erzielen werden. Wir ermutigen jeden, der über eine Freiwilligenarbeit nachdenkt, die Risiken und Vorteile abzuwägen und sich von klugen Leuten, denen Sie vertrauen, beraten zu lassen, bevor Sie sich anmelden.
Unsere Einschätzung zu AMT-130: Die erste Studie zur Huntingtin-senkenden Gentherapie hat das Potenzial, den Weg für eine neue Generation wirklich revolutionärer Medikamente zu ebnen. Diejenigen, die teilnehmen, sind nicht weniger mutig als die Astronauten, die vor fast genau fünfzig Jahren die Oberfläche des Mondes betraten. Unter erheblichem persönlichem Risiko werden sie sich freiwillig melden, um einen nicht so kleinen Schritt ins Unbekannte zu wagen, in der Hoffnung, einen Riesensprung für HD-Familien zu erzielen.
Wir werden weitere Updates über dieses und andere Huntingtin-senkende Programme veröffentlichen, sobald sie sich entwickeln.
Mehr erfahren
Quellen & Referenzen
Weitere Informationen zu unseren Offenlegungsrichtlinien finden Sie in unseren FAQ…


