Verursacht ein "rostiges Scharnier“ die Huntington-Krankheit?
Kanadische Wissenschaftler haben herausgefunden, dass das mutierte Huntingtin-Protein unflexibler als normal ist.
 Von Professor Ed Wild 14. November 2013 Bearbeitet von Dr Jeff Carroll Übersetzt von Michaela Winkelmann Ursprünglich veröffentlicht am 27. August 2013
Von Professor Ed Wild 14. November 2013 Bearbeitet von Dr Jeff Carroll Übersetzt von Michaela Winkelmann Ursprünglich veröffentlicht am 27. August 2013
Herauszufinden wie das mutierte Huntingtin-Protein den Schaden verursacht, ist das zentrale Problem der Huntington-Forschung. Jetzt hat ein Team von kanadischen Forschern unter der Leitung von Dr. Ray Truant gezeigt, dass das Protein eine wichtige “Scharnier”-Funktion hat, die in den Zellen mit der Huntington-Mutation schlechter funktioniert. Eine spannende Sache, aber im Gegensatz zu dem, was man vielleicht gelesen hat, bedeutet es nicht, dass wir keine Mäuse mehr studieren müssen!
Huntingtin
Es ist ein großer Vorteil für die Forscher, die die Huntington-Krankheit studieren, dass man im Gegensatz zu vielen anderen Gehirnerkrankungen genau weiß, was sie verursacht. Eine Mutation in einem einzigen Gen sagt den Zellen, ein schädliches Protein herzustellen: mutiertes Huntingtin. Es ist das mutierte Huntingtin, das den Neuronen und anderen Zellen schadet, was die Symptome der Huntington-Krankheit verursacht.
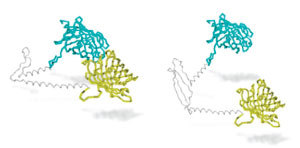
In den 20 Jahren seit seiner Entdeckung haben wir eine Menge darüber herausgefunden, was das Huntingtin-Protein normalerweise macht, und was schiefgeht, wenn sein giftiger Zwilling Huntingtin hergestellt wird.
Das Huntingtin zu studieren ist entscheidend für unsere Bemühungen, Behandlungen für die Huntington-Krankheit zu entwickeln, weil herauszufinden, wie und warum das mutierte Huntingtin Schaden verursacht, ein wichtiger Schritt in die Richtung ist, diesen Schaden zu verhindern.
Zu viele Glutamine
Proteine sind aus langen Ketten von Bausteinen gemacht, die Aminosäuren genannt werden. Diese werden wie Perlen auf einer Kette verbunden, und die genaue Reihenfolge der Aminosäuren bestimmt die Form und das Verhalten des Proteins.
Eine kleine Veränderung in der Reihenfolge der Aminosäuren kann eine große Veränderung der Form eines Proteins verursachen, und das kann dramatisch verändern, wie es seine Aufgabe in den Zellen erledigt oder es sogar giftig machen.
Das mutierte Huntingtin unterscheidet sich von dem "normalen” Protein in nur einer Art und Weise: in der Nähe des Anfangs der Zeichenfolge hat das Huntingtin-Protein eine Sequenz, in der ein Baustein, das Glutamin, mehrmals wiederholt wird. Die übliche Anzahl an Glutaminen liegt zwischen zehn und zwanzig.
Die Huntington-Krankheit tritt auf, wenn es zu viele Glutamine gibt.
Was ist die magische Zahl?
Wie viele Glutamine braucht es also, bis das Huntingtin-Protein beginnt, den Schaden zu verursachen? Seltsamerweise ist die Antwort siebenunddreißig. Darunter verursacht das Huntingtin-Protein die Huntington-Krankheit nicht – so weit man weiß. Darüber ist die Huntington-Krankheit unvermeidlich, solange eine Person lange genug lebt.
Warum in aller Welt verändern sich die Dinge bei 37 Glutaminen? Wir wissen es nicht! Aber dieses Geheimnis zu entwirren hat oberste Priorität für die Huntington-Forscher.
Noch seltsamer ist, dass während die meisten Menschen mit der Huntington-Krankheit zwischen 40 und 60 Glutaminen haben, produziert diese Anzahl an zusätzlichen Glutaminen bei anderen Tieren wie Mäusen die Krankheit nicht. Tiermodelle der Huntington-Krankheit brauchen gut über hundert Glutamine in ihrem Huntingtin-Protein, bevor man beginnt, die Symptome zu sehen.
Dies ist ein weiteres Geheimnis, und eines das nahelegt, dass das Huntingtin feine, aber sehr wichtige chemische Probleme bei den Menschen verursacht, die unsere Tiermodelle nicht erkennen.
Was ist mit dem CAG?
„Menschliche Zellen könnten verwendet werden, um die Medikamente zu identifizieren, die dem Scharnier dabei helfen zu funktionieren, aber sie müssen noch an Tieren getestet werden, einschließlich Mäusen “
Woher kommen diese zusätzlichen Glutamine, könnte man sich fragen. Die Antwort liegt im Huntington-Gen, das ist ein Rezept oder eine Reihe von Anweisungen zur Herstellung des Huntingtin-Proteins. So wie das Protein am Anfang viele Glutamine hat, so hat das Gen eine Streckung, wo die chemischen “Buchstaben” CAG wiederholt werden. Die Anzahl der „CAG“-Wiederholungen im Gen entspricht der Anzahl an Glutamin-Bausteinen im Protein. Und wenn es zu viele CAGs im Gen sind, werden es zu viele Glutamine im Huntingtin-Protein sein.
Was ist also neu?
Professor Ray Truant, sein Student Nick Caron und Truant’s Team an der McMaster University in Kanada haben gerade einen Artikel in der Zeitschrift PNAS veröffentlicht, der ihre Arbeit beschreibt, bei der sie untersuchen, wie die Anzahl der Glutamine auf das Huntingtin-Protein wirkt. Zum ersten Mal haben sie eine potenziell wichtige Veränderung gefunden, die um die kritische Glutamin-Zahl 37 auftreten.
Die Strecken des Proteins auf beiden Seiten all dieser Glutamine sind Stücke, die “Upstream” und “Downstream”-Regionen genannt werden. Frühere Forschung hat nahegelegt, dass jede von diesen einen Teil dabei spielt, um dem mutierten Protein seine schädlichen Eigenschaften zu geben.
Was Truant’s Team machte, war zu fragen, ob die Up- und Downstream-Regionen tatsächlich zusammenarbeiten könnten, mit dem Glutamin-Stück dazwischen, dass sich wie ein Scharnier verhält. Sie fragten sich auch, ob sein “Scharnier” in dem mutierten Protein möglicherweise nicht ordnungsgemäß funktioniert.
Zeit für eine „Herr der Ringe“-Analogie
Um dies zu untersuchen, brauchten sie einen Weg, um herauszufinden, ob die Up- und Downstream Regionen nahe genug kommen, um zusammenzuarbeiten. Sie verwendeten eine clevere Art von “Annäherungssensor” namens FLIM-FRET.
Erinnern Sie sich an Frodo‘s Schwert „Sting“ in den Herr der Ringe-Filmen, und wie es blau leuchtet, wenn Orks in der Nähe sind? FLIM-FRET ist so ähnlich.
Die Forscher steckten spezielle lichtempfindliche Anhängsel an das Huntingtin-Protein, eins an die Upstream Region und eins an die Downstream Region. Diese machen nichts, solange bis sich das Protein faltet, um die beiden Regionen zusammenzubringen. Wenn das geschieht, wird Licht von einem Anhängsel an das andere übergeben, es strahlt (wie Frodo‘s Schwert) und kann gemessen werden.
Das rostige Scharnier der Huntington-Krankheit
Truant‘s Sting-ähnlicher Annäherungssensor bewies, dass die Up- und Downstream Regionen am Ende in die Zellen gelangt sind, mit der Glutamin-Streckung, die wie ein Scharnier wirkt. Außerdem leuchtete es weniger hell, wenn es 37 oder mehr Glutamine im Huntingtin gibt, was darauf hindeutet, dass die Probleme mit dem Scharnier um diese Zahl beginnen. Truant nennt dies die “rostige Scharnier-Hypothese” und schlägt vor, dass es eine Möglichkeit ist, wie das mutierte Protein den Schaden verursachen könnte.
Truant‘s Team bestätigte diese Ergebnisse, indem sie Proteine verschiedener Längen verwendeten und schließlich die gleiche Anomalie in direkt von Huntington-Patienten entnommenen Hautzellen zeigten.
Anknüpfung

Wie passt die „rostige Scharnier“ Idee mit anderen Dingen zusammen, die wir bereits über das mutierte Huntingtin wissen? Nun, wir wissen, dass ein anderes Protein namens PACSIN an der Downstream Region des Huntingtin‘s festkleben kann. Hier zeigte Truant‘s Team, das es auch an der Upstream Region festkleben kann, was nahelegt, es könnte vielleicht in der Lage sein, die beiden Regionen über das Glutamin-Scharnier zusammenzuhalten - wie ein Türschließmechanismus.
Wenn das PACSIN künstlich entfernt wurde, glühte der Annäherungssensor weniger, was darauf hindeutet, dass die Up- und Downstream Regionen auseinander gesprungen waren. Das Verhalten von PACSIN zu verändern könnte das Scharnierproblem überwinden - ein möglicher neuer Ansatz, um über die Behandlung der Huntington-Krankheit nachzudenken.
Der andere Anknüpfungspunkt zu unserem vorhandenen Verständnis kommt von kleinen chemischen Veränderungen, die den Zellen sagen, die Proteine herzustellen. Diese chemischen “Tags” können verändern, wie sich die Proteine verhalten und wohin sie gelangen. Truant’s Team hatte zuvor gezeigt, dass „Phospho“-Tags wichtig sind für die Bestimmung, wohin das Huntingtin-Protein gelangt und wie schädlich es ist.
In ihrer neuesten Arbeit zeigten sie, dass diese Phospho-Tags auch einen Einfluss auf die Aktivität des Glutamin-Scharniers haben können. Dies bietet weitere Unterstützung für die Idee, dass Medikamente zur Steuerung des Phospho-Taggings einige der schädlichen Auswirkungen des mutierten Proteins verhindern könnten.
Was diese Studie zeigt
Truant’s Team hat wirklich gute Arbeit geleistet, um einen Annäherungssensor zu erfinden (oder einen von Frodo Beutlin auszuleihen) und ihn zu nutzen, um zu zeigen, dass Huntingtin’s entscheidende Glutamin-Region - das Stück, das bei der Huntington-Krankheit zu lang ist - als Scharnier fungiert, um der Up- und Downstream Region zu ermöglichen zusammenzuarbeiten.
Während ein anderes Protein, PACSIN, das Scharnier spannt und es zusammenzieht. Und sie haben die Scharnierfunktion mit dem Phospho-Tagging von Huntingtin verknüpft. Außerdem scheint diese Scharnier-Eigenschaft ab etwa der gleichen Anzahl von Glutaminen falsch zu laufen, die die Krankheit bei menschlichen Patienten verursacht.
Dies ist nicht nur eine neue Information über das Huntingtin-Protein, und wie es den Schaden verursacht. Es gibt uns auch neue Ideen für mögliche Behandlungen - durch die Veränderung des Verhaltens von PACSIN1 oder der Maschinerie, die das Phospho-Tagging regelt.
Was sie nicht zeigt
Dies wäre kein HDBuzz-Artikel ohne ein Wort der Warnung. In diesem Fall halten wir es für wichtig, einige der Dinge hervorzuheben, die die Forschung nicht sagt - im Gegensatz zu dem, was man vielleicht online lesen kann.
CBC News berichtet, dass die Arbeit “die Notwendigkeit für Mausstudien umgeht“, weil Truant‘s Feststellungen in menschlichen Zellen gesehen werden konnten. Leider ist das nicht wahr. Menschliche Zellen könnten verwendet werden, um schnell Medikamente zu identifizieren, die dem „Scharnier“ helfen, besser zu arbeiten, aber diese Medikamente müssen noch an Tieren getestet werden einschließlich Mäusen. Um die Huntington-Krankheit zu besiegen, benötigen wir alle Hilfe, die wir bekommen können. Kein einziges Tiermodell ist für die Entwicklung von Medikamenten perfekt - menschliche Zellen wachsen weder in einer Petrischale noch auf eigene Faust. Verschiedene Modellsysteme tragen jeweils nützliche Informationen dazu bei, um uns zu helfen, Fortschritte zu machen.
Eine andere Sache, die uns diese Arbeit gibt, ist ein umfassendes Verständnis davon, wie das Scharnier-Problem verursacht, dass das Huntingtin-Protein schädlich wird. Ein großer Teil der Zeit in der Forschung, hinter jeder Tür finden wir eine weitere Tür, die mehr Arbeit braucht, um sich zu öffnen. Truant’s Team und andere werden jetzt an dem Verständnis des größeren Bildes arbeiten, davon wie das Huntingtin-Scharnier-Problem die Funktionsweise der Zelle und des Gehirns betrifft. Und diese Erkenntnisse in Behandlungen umzuwandeln, die von den Patienten eingenommen werden, braucht noch mehr Arbeit. Wir lassen uns also nicht unterkriegen!


