
Roche gibt Details zu seiner „entscheidenden“ Studie zur Senkung des Huntingtin-Wertes bekannt
In der GENERATION-HD1-Studie wird untersucht, ob RG6042 – ehemals Ionis-HTTRx – das Fortschreiten der Huntington-Krankheit verlangsamt

Es ist eine Zeit großer Entwicklungen auf dem Gebiet der Huntingtin-senkenden Medikamente, die darauf abzielen, die Produktion des Huntingtin-Proteins zu reduzieren, das die Huntington-Krankheit verursacht. Auf der Tagung des European Huntington’s Disease Network (EHDN) in der vergangenen Woche gab Roche konkrete Details zur ersten entscheidenden Studie mit einem Huntingtin-senkenden Medikament bekannt – RG6042, das Sie vielleicht besser als Ionis-HTTRx kennen. Was wissen wir also über die Studie?
Was bedeutet Huntingtin-Senkung?
Zunächst eine kurze Zusammenfassung über die Huntingtin-Senkung als Behandlung der Huntington-Krankheit. Denken Sie daran, dass die Schädigung des Gehirns bei HD durch ein schädliches Protein verursacht wird, das als mutiertes Huntingtin bezeichnet wird. Das HD-Gen – manchmal auch Huntingtin-Gen genannt – ist ein Rezept für die Herstellung des Huntingtin-Proteins.

Wenn eine Zelle mehr von einem bestimmten Protein benötigt, beispielsweise dem Huntingtin-Protein, erstellt sie eine Art Scratch-Kopie des Gens – ein Botenmolekül, das mit einer etwas anderen Chemikalie, der RNA, geschrieben wird. Da diese RNA eine Nachricht trägt, bezeichnen Wissenschaftler sie als Boten-RNA oder mRNA. Jede Unterbrechung dieser Kette, vom Gen über den Boten zum Protein, und die Zelle würde kein spezifisches Protein herstellen.
So funktionieren Huntingtin-senkende Ansätze zur Behandlung von HD – indem sie auf die Huntingtin-Boten-RNA abzielen und den Zellen signalisieren, sie zu ignorieren oder zu löschen. Weniger Nachricht, weniger Protein.
Die meisten HD-Forscher finden diesen Ansatz sehr aufregend, da der gesunde Menschenverstand und eine Menge Tierforschung darauf hindeuten, dass eine Reduzierung oder Eliminierung des mutierten Huntingtin-Proteins die Schwere der HD-Symptome verringert.
ASOs bei der Huntington-Krankheit
Ein früher Vorreiter auf dem Gebiet der Huntingtin-Senkung ist ein Biotech-Unternehmen namens Ionis Pharmaceuticals aus Carlsbad, Kalifornien. Im Laufe der Jahrzehnte haben sie einen Ansatz entwickelt, der als Antisense-Oligonukleotide bezeichnet wird. Dabei handelt es sich um stark modifizierte DNA-ähnliche Moleküle, die so programmiert sind, dass sie nur eine bestimmte Boten-RNA erkennen, die in einer Zelle herumschwirrt.
Wenn diese ASOs an ihrem programmierten Ziel haften, zerstören die Zellen es, wodurch die Konzentrationen einer bestimmten Boten-RNA drastisch reduziert werden. Weniger Botenstoff bedeutet weniger Protein, auch wenn der genetische Code für das Huntingtin-Gen immer noch in der DNA vorhanden ist.
Basierend auf dem Erfolg in Tierversuchen leitete Ionis ab 2015 eine erste Studie mit 46 mutigen freiwilligen HD-Patienten. Diese kleine Studie sollte lediglich feststellen, ob ihr Huntingtin-senkendes Medikament namens HTTRx sicher ist und ob die Behandlung mit HTTRx die Produktion des Huntingtin-Proteins im Nervensystem reduziert. Wir können keine Hirngewebeprobe entnehmen, aber wir können die Konzentrationen des mutierten Huntingtin-Proteins in der Rückenmarksflüssigkeit messen, die das Gehirn umgibt.
Wie auf HDBuzz diskutiert, gaben Ionis und sein Partner Roche im Dezember 2017 bekannt, dass die Studie ein Erfolg gewesen war. Bemerkenswerterweise hatte keiner der 46 Patienten die Studie abgebrochen, trotz der monatlich erforderlichen Injektionen in die Rückenmarksflüssigkeit. Und noch bemerkenswerter war, dass die Behandlung mit HTTRx zu einer deutlichen Reduktion der Konzentrationen des Huntingtin-Proteins in der Rückenmarksflüssigkeit führte.
Roche ist ein riesiges Pharmaunternehmen mit Sitz in der Schweiz, dessen US-amerikanischer Zweig Genentech heißt. Neben den guten Nachrichten aus der ersten Studie bestätigte Roche, dass es die nächste Studie mit HTTRx planen und leiten würde, die es im Rahmen der Übergabe in RG6042 umbenannte. Gewöhnen Sie sich an Geschichten über RG6042 – aber denken Sie daran, dass es sich um dasselbe HTTRx-Medikament handelt, für das wir die ganze Zeit die Daumen gedrückt haben.
Eine Studie zur Prüfung der Wirksamkeit
Natürlich sind sowohl Forscher als auch die Huntington-Krankheits-Community daran interessiert, das Fortschreiten von HD zu verlangsamen und nicht die Konzentrationen einer bestimmten Messung in der Rückenmarksflüssigkeit zu verändern. Die erfolgreiche Sicherheitsstudie von Ionis umfasste jedoch nur drei Monate Dosierung bei 46 Patienten – das ist zu kurz und zu klein, um festzustellen, ob die Behandlung Auswirkungen auf die HD-Symptome hatte.
„GENERATION-HD1 wird Ende 2018 starten, wobei die ersten Patienten Anfang 2019 aufgenommen werden. Sie wird an rund 80-90 Standorten in etwa 15 Ländern stattfinden.“
Nachdem wir nun wissen, dass das Medikament von Ionis/Roche das Protein senkt und anscheinend sicher ist, benötigen wir nun eine große Studie mit einer viel größeren Personengruppe – eine sogenannte Phase-3-Studie –, um festzustellen, ob RG6042 das Fortschreiten der Huntington-Krankheit verlangsamt.
Seit Dezember warten wir gespannt auf eine Ankündigung zu dieser größeren Studie. Und am 16. September war es so weit!
GENERATION-HD1
Auf der Tagung des European Huntington’s Disease Network (EHDN) 2018 gab Scott Schobel von Roche den ersten offiziellen Überblick über die bevorstehende Studie. Die Studie wird als GENERATION-HD1 bekannt sein.
(Der Name GENERATION-HD1 kommt von Global EvaluatioN of Efficacy and safety of Roche/genentech AnTIsense OligoNucleotide for Huntington’s Disease. Am besten merken Sie sich einfach das Akronym…)
Die Größe ist wichtig
GENERATION-HD1 wird Ende 2018 starten, wobei die ersten Patienten Anfang 2019 aufgenommen werden. Sie wird an rund 80-90 Standorten in rund 15 Ländern stattfinden.
Es wurden noch keine spezifischen Standortankündigungen gemacht, was bedeutet, dass es noch keine öffentlichen Informationen darüber gibt, ob eine bestimmte Klinik oder sogar ein Land die Studie durchführen wird. Wir gehen davon aus, dass diese Informationen bald verfügbar sein werden.
Es wird eine sehr große Studie sein – mit der Aufnahme von 660 Patienten mit manifestem HD. „Manifeste HD“ bedeutet einfach, dass Personen aufgenommen werden, bei denen formell klinische Anzeichen und Symptome von HD diagnostiziert wurden, nicht Personen mit der Mutation, aber ohne eindeutige Symptome (prämanifeste oder prodromale HD).
Teilnahmeberechtigung
Es gibt zwei wichtige klinische Entscheidungsträger oder Einschlusskriterien. Erstens müssen die Patienten „gehfähig“ und „sprachfähig“ sein – das heißt, in der Lage sein, zu gehen und zu sprechen. Zweitens müssen sie bei einem unabhängigen Test namens Functional Assessment 70 % oder mehr erreichen. Das bedeutet ein Maß an täglicher Funktionsfähigkeit, bei dem sie sich waschen und „begrenzte“ Haushaltsarbeiten wie Kochen und die Verwendung eines Messers verrichten können.
Dies sind viel umfassendere klinische Einschlusskriterien als in der vorherigen Studie, die sehr streng auf sehr frühe HD mit nahezu normaler täglicher Funktionsfähigkeit beschränkt war.
Es gibt auch eine spezifische Anforderung, dass ein sogenannter CAP-Score über einem bestimmten Wert liegen muss.
Der CAP-Score ist eine einfache mathematische Methode, um das Alter einer Person und ihre CAG-Repeat-Anzahl zu kombinieren – die Länge des abnormalen DNA-Abschnitts, der die Huntington-Krankheit verursacht. Dieser Score wird verwendet, weil Menschen mit schwerwiegenderen HD-Mutationen (längere CAG-Repeats) tendenziell in jüngerem Alter HD-Symptome aufweisen. Wenn wir also das Fortschreiten der HD-Symptome im Laufe der Zeit bei einer Person verfolgen möchten, müssen wir sowohl ihr Alter als auch ihre CAG-Größe berücksichtigen. Das Festlegen einer Mindestanforderung an den CAP-Score bedeutet, dass sich die Studie auf Personen konzentrieren kann, bei denen die Wahrscheinlichkeit am größten ist, dass sie von dem Medikament profitieren, wodurch sie so klein und schnell wie möglich wird.
Viele Lumbalpunktionen
Die Studie umfasst eine Placebo– oder Scheinbehandlungsgruppe, die etwa ein Drittel der Studienteilnehmer ausmacht. Diese Gruppe ist unbedingt erforderlich, um mit dem Placebo-Effekt fertig zu werden – der Tatsache, dass die Teilnahme an einer solchen Studie dazu führt, dass sich die Menschen besser fühlen und sogar besser funktionieren, selbst wenn das Medikament nicht wirkt.
Die anderen zwei Drittel der Teilnehmer werden in zwei Gruppen aufgeteilt, die beide das aktive Medikament erhalten. Die Hälfte der behandelten Gruppe erhält das Medikament jeden Monat und die andere Hälfte jeden zweiten Monat. Das ist aufregend, weil wir so möglicherweise seltener behandeln können, wenn sich dies als ebenso wirksam wie die monatliche Dosierung erweist.
Alle Teilnehmer in jeder Gruppe müssen sich jedoch zwei Jahre lang jeden Monat Injektionen in die Rückenmarksflüssigkeit verabreichen lassen. Die Placebo-Gruppe erhält jeden Monat eine Placebo-Injektion. Die monatliche Medikamentengruppe erhält jeden Monat das Medikament. Und die zweimonatliche Gruppe wechselt zwischen Medikamenten- und Placebo-Injektionen ab. Das bedeutet, dass niemand weiß, welcher Gruppe er zugeteilt wurde.
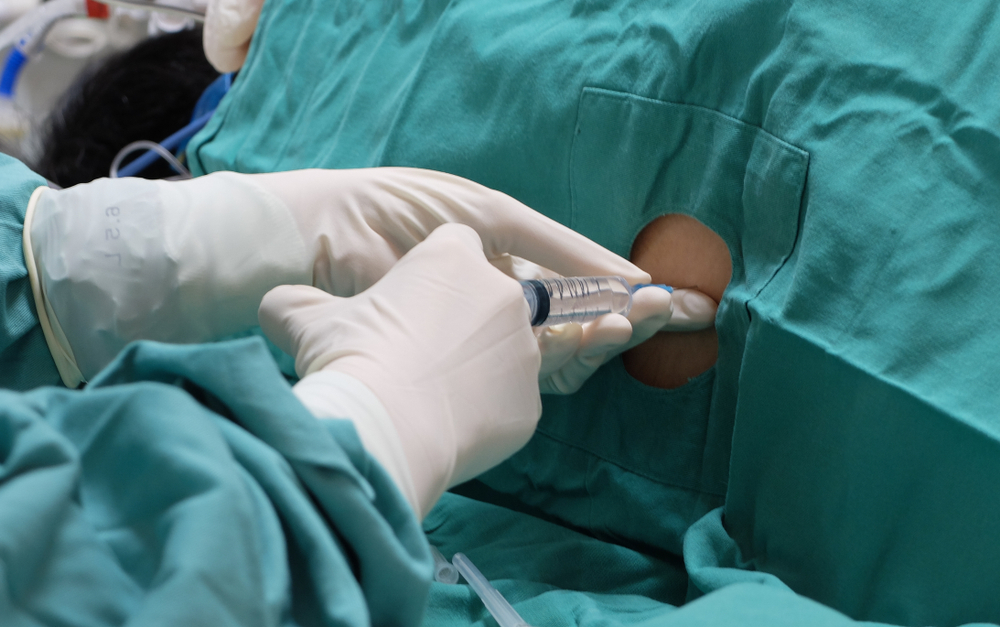
Fazit: Jeder Teilnehmer an der Studie muss damit einverstanden sein, viele Spinal Taps und spinale Injektionen zu erhalten – bis zu fünfundzwanzig über zwei Jahre.
Ergebnisparameter
Erfolg oder Misserfolg in der Studie wird in den USA durch eine Skala namens Total Functional Capacity oder kurz TFC bestimmt. Dies ist eine sehr einfache Bewertungsskala, die auf der Fähigkeit einer Person basiert, grundlegende Aufgaben im Haushalt, bei der Arbeit und bei der Selbstversorgung zu erledigen.
In Europa wird in der Studie ein etwas ausgefeilteres Maß verwendet, die sogenannte Composite Unified Huntington’s Disease Rating Scale oder cUHDRS. Dieser Score berücksichtigt ein breiteres Spektrum an HD-Symptomen und kombiniert die TFC, einen Bewegungsscore und einige Denkübungen.
„Es wird eine sehr große Studie sein – mit der Aufnahme von 660 Patienten mit manifestem HD.“
Es ist etwas ungewöhnlich, aber nicht unbekannt, eine Studie mit unterschiedlichen Endpunkten in verschiedenen Ländern durchzuführen. Aber diese Scores messen alle denselben zugrunde liegenden Prozess, nämlich die Verschlechterung von HD im Laufe der Zeit, und die verschiedenen Aufsichtsbehörden scheinen unterschiedliche Meinungen darüber zu haben, wie dies am besten gemessen werden kann. Am Ende würden wir erwarten, dass sich beide Scores in die gleiche Richtung bewegen, wenn das Medikament wirkt.
Nicht jeder Patient nimmt am ersten Tag der Studie teil, daher dauert eine Studie, an der jeder Teilnehmer 25 Monate lang teilnimmt, etwa doppelt so lange und möglicherweise noch länger.
Aber warten Sie, es gibt noch mehr
Roche kündigte auch eine weitere Studie an – die sogenannte Natural History Study, die darauf abzielt, wichtige Informationen über das Fortschreiten von HD zu liefern. Es werden bis zu 100 Patienten aufgenommen, die mit Teilnehmern der bereits laufenden Open-Label-Extension-Studie von RG6042 übereinstimmen. Bei diesen Open-Label-Teilnehmern handelt es sich um die Personen aus der ersten klinischen Studie, die nun alle regelmäßig das Medikament erhalten, sodass die Natural-History-Studie dazu beitragen wird, die aus der Open-Label-Studie gewonnenen Daten zu verstehen. Wenn alles nach Plan verläuft, wird den Teilnehmern der Natural-History-Studie nach 15-monatiger Teilnahme, einschließlich regelmäßiger Lumbalpunktionen, ebenfalls eine Open-Label-Behandlung angeboten.
Und noch mehr!
Die EHDN-Tagung umfasste Updates zu anderen aufregenden Huntingtin-senkenden Programmen, darunter Wave Life Sciences, PTC Therapeutics und Uniqure. Wir werden in Kürze Updates zu diesen und anderen Neuigkeiten von der EHDN 2018 bereitstellen.
Was nun?
Nach der ersten Studie, die die kurzfristige Sicherheit und die erfolgreiche Huntingtin-Senkung demonstrierte, haben wir nun solide Details über eine „entscheidende“ Studie, um zu beweisen, ob RG6042 wirkt oder nicht, und einen sehr klaren Zeitplan, wann dies geschehen wird.
Es ist wichtig zu bedenken, dass die Menschen, die an GENERATION-HD1 teilnehmen, einen langen und herausfordernden Weg vor sich haben werden und die Teilnahme körperlich und geistig anstrengend sein wird.
Unweigerlich wird es auch viele Menschen geben, die aus einer Reihe von Gründen nicht teilnehmen können. Auch wenn dies für diese Menschen sehr enttäuschend sein mag, wird das Medikament von Freiwilligen auf der ganzen Welt getestet, und es ist wichtig, sich daran zu erinnern, dass der Zweck der Studie darin besteht, das Medikament für alle und für zukünftige Generationen zu testen – und nicht, das Medikament an eine einzelne Person zu verabreichen.
Dennoch sind dies großartige Neuigkeiten. Nach jahrelanger Arbeit von Hunderten von Menschen haben wir endlich einen Zeitplan, um zu verstehen, ob die Behandlung mit diesem Huntingtin-senkenden Medikament RG6042 die HD-Symptome lindern könnte.
Wir freuen uns sehr über diese Ankündigung und den Zustand des Huntingtin-senkenden Bereichs im Allgemeinen. Wir halten es für fair, wenn die Mitglieder der HD-Community genauso empfinden. Bleiben Sie auf HDBuzz auf dem Laufenden, um Updates zu dieser und anderen Studienentwicklungen zu erhalten.
Mehr erfahren
Weitere Informationen zu unseren Offenlegungsrichtlinien finden Sie in unseren FAQ…


