
"Huntington’s Disease Therapeutics" Konferenz 2023 – Tag 2
Lesen Sie die neuesten Forschungsergebnisse von Tag 2 der "Huntington’s Disease Therapeutics" Konferenz 2023 #HDTC2023


Willkommen zum zweiten vollen Tag der HK-Wissenschaft, live aus Dubrovnik! Nach den erstaunlichen Vorträgen zur Grundlagenforschung von gestern beginnt der heutige Tag mit einer Sitzung, die sich auf Unternehmen konzentriert, die neue experimentelle Behandlungen für die HK entwickeln.
Unsere Twitter-Updates sind unten zusammengestellt. Folgen Sie die Live-Updates für den Rest der Konferenz mit dem Hashtag #HDTC2023.
Sehen Sie sich unsere Berichterstattung über Tag 1 hier an: https://de.hdbuzz.net/343. Wir werden für jeden Tag der Konferenz Zusammenfassungen im Artikelformat veröffentlichen.
Therapie Kandidaten für die HK
Ein einzigartiger Ansatz für ASOs
Die erste Rednerin des Vormittags ist Dr. Nicole Datson von der Firma VICO, die mit einer Art von Medikamenten arbeitet, die vielen Huntington-Familien bekannt ist: Antisense-Oligonukleotide (ASOs). Mehrere Unternehmen, darunter Wave Life Sciences und Roche, testen bereits ASO-Medikamente bei der HK, doch der Ansatz von Vico ist einzigartig. VICOs ASO zielt direkt auf die genetische Mutation, die die HK verursacht – eine erweiterte „CAG“-Sequenz am Anfang des Huntingtin-Gens. Dies hat sehr interessante Auswirkungen, denn die Huntington-Krankheit ist nicht die einzige „CAG-Repeat-Expansion“-Krankheit – mindestens acht weitere menschliche Krankheiten werden durch genau dieselbe genetische Veränderung verursacht, allerdings in verschiedenen Genen des Genoms. Wenn das Medikament also funktioniert, könnte es potenziell bei jeder dieser Krankheiten eingesetzt werden, die mit der gleichen genetischen Veränderung einhergehen.
Dr. Nicole Datson, Chief Scientific Officer von Vico, gibt einen Überblick über den Ansatz von Vico. Selbst das normale Huntingtin-Gen hat eine lange CAG-Sequenz (~17-20 bei den meisten Menschen ohne Huntington), so dass es für diese Medikamente schwierig ist, nur die Krankheitsform von Huntingtin spezifisch zu binden. Vico weist jedoch darauf hin, dass seine ASOs, die auf die CAG-Sequenz abzielen, zwar nicht nur die längere Form erkennen, die die Krankheit verursacht, dass sie aber diese längeren CAG-Sequenzen zu bevorzugen scheinen, so dass die Wirkung des Medikaments auf die erweiterte CAG-Wiederholung stärker ist. Nicole zeigt ihre Daten von Zellen von Huntington-Patienten nach der Behandlung mit ihrem ASO-Medikament, das sie kurz VO659 nennt. Die Behandlung mit höheren ASO-Dosen führt zu einer stärkeren Reduzierung des erweiterten Huntingtin-Proteins, dem Bösewicht der Huntington-Krankheit.
Interessanterweise hat dasselbe ASO auch Auswirkungen auf Zellen von Patienten mit zwei anderen Gehirnkrankheiten, die eine CAG-Expansion aufweisen, nämlich die Ataxieformen SCA1 und SCA3. In beiden Fällen bevorzugt das ASO auch die mutierte Form des Gens mit den längeren CAG-Wiederholungen. Wenn es funktioniert, könnte ein einziges Medikament für eine ganze Reihe von Krankheiten eingesetzt werden, die durch CAG-Wiederholungen verursacht werden, darunter HK, SCA1, SCA3, DRPLA und SBMA.
Abgesehen von den Zellen zeigt Nicole, dass die Behandlung von Mäusen mit schwerer Huntington-Erkrankung mit ASO auch zu einer Verringerung des Huntingtin-Proteins führt. Auch das Verhalten und die Hirnanatomie der HK-Mäuse wurden durch die ASO-Behandlung verbessert – sehr cool. Vicos Daten zeigen, dass das ASO lange im Gehirn der Tiere verbleibt, was darauf hindeutet, dass die Abstände zwischen den Behandlungen recht groß sein könnten. Dies wäre ein großer Vorteil für ASOs, die in die Wirbelsäule injiziert werden müssen, um das Gehirn zu erreichen.
In Mausmodellen für zwei andere CAG-Expansionskrankheiten, SCA1 und SCA3, konnten sie ähnliche Vorteile feststellen: Die Krankheitsversionen des Gens wurden in größerem Umfang ausgeschaltet, was zu einer Verbesserung der krankheitsähnlichen Symptome führte. VICO hat sein Medikament auch an Affen getestet und konnte feststellen, dass es sich in den verschiedenen Hirnregionen recht gut ausbreitet und lange im Gehirn verbleibt, wie es auch bei den Mäusen der Fall war. Auf der Grundlage der Daten aus den Tierversuchen ist Vico der Ansicht, dass das Medikament sowohl bei der Huntington-Krankheit als auch bei anderen Krankheiten nur ein paar Mal pro Jahr injiziert werden müsste. Dies würde die Behandlung für die Familien wesentlich einfacher machen und die Teilnahme an der Studie erleichtern. Angesichts dieser vielversprechenden Tier- und Zellstudien hat Vico eine frühe Humanstudie an Patienten mit der Huntington-Krankheit, SCA1 und SCA3 eingeleitet – sehr cool, dass sie diese Krankheiten alle in einer einzigen Studie behandeln.
RNA-Interferenz
Als nächstes spricht Dr. William Cantley, Forscher bei Alnylam Pharmaceuticals, einem führenden Unternehmen auf dem Gebiet der „RNA-Interferenz“, auch RNAi genannt. Dies ist eine völlig andere Chemie als ASOs, hat aber ein sehr ähnliches Ziel – die Verringerung der Konzentration eines Zielproteins. Theoretisch ist RNAi wirksamer als ASOs, d. h. man braucht weniger Arzneimittel für die gleiche Wirkung, aber bisher werden ASOs in großem Umfang bei Hirnerkrankungen eingesetzt. Ein Teil des Problems ist die Verabreichung – wie kann man RNAi-Medikamente zu den 84 Milliarden Gehirnzellen bringen, die bei der HK behandelt werden müssten. Um RNAi-Medikamente in andere Zelltypen wie die Leber zu bringen, wurden kleine molekulare Schlüssel auf RNAi-Medikamente geklebt. Wenn Zellen im Körper ein passendes Schloss auf ihrer Zelloberfläche haben, können sie RNAi-Medikamente viel leichter aufnehmen. Alnylam hat viel Erfahrung mit diesen Schlüssel-Schloss-Tricks, um RNAi-Medikamente in Leberzellen zu bringen. Die Behandlung der Leber ist bei der HK jedoch weniger wichtig. Deshalb hat Alnylam einen neuen Schlüssel, „C16“, entwickelt, der wichtige Gehirnzelltypen freischaltet, die uns bei der HK wichtig sind.
William zeigt sehr interessante Daten zu einer anderen Hirnerkrankung, der Alzheimer-Krankheit, bei der die Markierung eines RNAi-Medikaments mit C16 sehr gut zu funktionieren scheint, um in die Gehirne von Affen zu gelangen. William kündigt – zum ersten Mal öffentlich – an, dass Alnylam an einem RNAi-Medikament gegen Alzheimer arbeitet und dabei diesen coolen neuen C16-Schlüsselansatz verwendet.
Nachdem er das Publikum durch den strategischen Entscheidungsprozess von Alnylam geführt hat, gibt William einen Überblick über einige frühe Arbeiten mit einem neuen C16-RNAi-Medikament an Mäusen mit der HK. Mit zwei verschiedenen Medikamenten, die auf unterschiedliche Teile des HK-Gens abzielen, wurde eine Verringerung des Huntingtin-Proteins festgestellt. Zusätzlich zu diesen Studien an HK-Mäusen hat Alnylam auch Studien an Affengehirnen durchgeführt, die eine sehr starke Verringerung des HTT-Proteinspiegels im Kortex, dem faltigen äußeren Teil des Gehirns, der von der HK betroffen ist, zeigen. Es ist spannend, einen weiteren Pfeil im Köcher der HTT-senkenden Medikamente zu haben, denn RNAi-Medikamente und ASO-Medikamente haben unterschiedliche Risiken und Vorteile. Wir werden erst dann wissen, welcher dieser Ansätze den größten Nutzen bringt, daher ist es gut, einen weiteren Teilnehmer im Rennen zu haben.
Herstellung eines Huntingtin-Protein-Abbauers
Der letzte Vortrag vor der ersten Kaffeepause des Tages kommt von Adam Hendricson, der bei Arvinas Operations arbeitet. Adam wird uns über die Arbeit an der Herstellung eines Huntingtin-Protein-Abbauers berichten – ein Medikament mit kleinen Molekülen, das die Huntingtin-Konzentration reduzieren kann, indem es in den Mülleimer der Zelle geschickt wird.
In den letzten Jahren hat es eine wissenschaftliche Explosion bei einer neuen Art von Technologie gegeben, die sich auf den Abbau von Krankheitsproteinen mit kleinen Molekülen, den so genannten PROTACs, konzentriert. Dies ist insofern interessant, als diese Medikamente, wenn sie sich bewähren, über den Mund eingenommen werden KÖNNEN. PROTACs funktionieren, indem sie ein Müll markierendes Protein in unseren Zellen in engen Kontakt mit einem Zielprotein bringen, in unserem Fall dem Huntingtin-Protein. Dies würde dazu führen, dass Huntingtin auf eine besondere Weise markiert wird, die der Zelle sagt, dass sie es wie Müll behandeln soll. Arvinas ist eines der ersten Unternehmen, das diese Technologie in eine klinische Studie einbringt. Sie testen derzeit eines ihrer Medikamente zur Behandlung von Krebs und zeigen damit, dass dieser neue Ansatz mehr sein kann als nur ein cooles Werkzeug für Laborwissenschaftler. Sie arbeiten an einer Reihe verschiedener Hirnerkrankungen, darunter Alzheimer, Parkinson und die Huntington-Krankheit.
Arvinas hofft, das „lösliche“ Huntingtin-Protein ins Visier nehmen zu können, also die Form, die der Bildung der fester strukturierten Proteinklumpen vorausgeht. Außerdem suchen sie nach Wirkstoffmolekülen, die das mutierte gegenüber dem normalen Huntingtin-Protein bevorzugen. In Zellen in einer Schale zeigen sie, dass das von ihnen identifizierte PROTAC sowohl an das mutierte Huntingtin-Protein als auch an das Protein mit der Müllmarkierung bindet. Diese Moleküle binden sehr fest, und das ist es, wonach Medikamentenjäger wie Adam suchen!

Das PROTAC-Molekül von Arvinas kann tatsächlich die Konzentrationen sowohl der löslichen als auch der verklumpten Form des erweiterten Huntingtins senken, was eine gute Nachricht ist, denn die Wissenschaftler glauben, dass eine Senkung der Konzentrationen beider Proteine für die Patienten von Vorteil wäre. Die meisten dieser Arbeiten wurden bisher an Zellen in einer Schale durchgeführt, aber Arvinas beginnen nun damit, ihr Molekül an Mäusen zu testen. Die gute Nachricht ist, dass PROTAC in der Lage zu sein scheint, in das Gehirn zu gelangen, was für Medikamente oft sehr schwierig zu erreichen ist.
Verfolgen der Übermenschen
Als nächstes hören wir von Dr. Donna Finch von Alchemab Therapeutics. Ihr Schwerpunkt liegt auf dem Immunsystem, wobei sie Antikörper einsetzen, die möglicherweise die Gehirnzellen bei der HK schützen könnten. Ihr Ansatz besteht darin, natürlich vorkommende schützende Antikörper bei Patienten zu finden, die resilient sind, d. h. sehr langlebig oder weniger von Krankheitsgenen betroffen. Dann führen sie alle möglichen Untersuchungen durch, um herauszufinden, warum ihre Antikörper schützend wirken, und testen die besten davon in Zellen und an Tieren.
Das ist so, als würde man die natürlichen „Übermenschen“ unter uns aufspüren und herausfinden, warum Krankheiten sie weniger zu beeinträchtigen scheinen als die meisten Menschen, und diese Informationen nutzen, um andere zu behandeln. Alchemab ist zu dieser Konferenz gekommen, um herauszufinden, wie sie ihren Ansatz für die Huntington-Krankheit nutzen können – es ist sehr aufregend, dass ein anderes Unternehmen kommt, um an einer neuen Art von Therapeutika zu arbeiten! Alchemab arbeitet mit Organisationen in der ganzen Welt zusammen, die ihnen geholfen haben, Proben von Menschen mit verschiedenen Krankheiten und Schwachstellen zu sammeln. Sie haben Informationen über das Immunsystem in einem „Datenwürfel“ zusammengefasst, der es ihnen ermöglicht, groß angelegte Analysen über viele Personen hinweg durchzuführen.
Wir leben im Zeitalter der Big Data! Unternehmen wie Alchemab nutzen riesige Datensätze und viele clevere Computertools, um kleine Signale in den Daten zu finden, die neue biologische Zusammenhänge aufdecken könnten. Sie haben herausgefunden, dass Antikörper gegen das Huntingtin-Protein bei widerstandsfähigen Personen gebildet werden, sogar bei anderen Krankheiten wie Alzheimer. Alchemab hat einen Antikörper mit der Bezeichnung ATLX-1095 identifiziert, der sich an ein Fragment des Huntingtin-Proteins bindet. Die Idee ist, dass dieser Antikörper das Immunsystem dazu bringen könnte, sich auf die Beseitigung des schädlichen Proteins zu konzentrieren.
In ersten Tests hat dieser Antikörper verhindert, dass Teile des schädlichen Huntingtins zusammenkleben und größere Klumpen bilden, die als giftig gelten. Alchemab arbeitet mit einer Reihe von akademischen Partnern zusammen, die diese Experimente nun wiederholen – eine tolle Partnerschaft! Alchemab hat auch gezeigt, dass ATLX-1095 die Menge der Huntingtin-Aufräumarbeiten erhöht, die von einer Art von Hilfszellen, den Mikroglia, durchgeführt werden. Das Medikament hilft also dabei, den Müll in den Zellen zu „verschlingen“, wie Donna es ausdrückt. Das Medikament ist auch in der Lage, in das Gehirn einzudringen. Während diese Antikörper ursprünglich direkt aus menschlichen Zellen stammen, müssen sie in größerem Maßstab hergestellt werden, um mehr Experimente und schließlich Studien am Menschen durchführen zu können. Alchemab hat erste Erfolge bei der Herstellung des Antikörpers im Labor erzielt. Jetzt wird dieses potenzielle Medikament an Mäusen getestet. Wir werden also an dieser Stelle die nächsten Phasen der präklinischen Arbeit verfolgen!
Zielgerichtetes Exon 1
Als nächstes ist Dr. Pavlina Konstantinova von VectorY an der Reihe. Das Unternehmen arbeitet an einer Reihe von verschiedenen Hirnerkrankungen, darunter ALS, Parkinson und Huntington. Wie viele andere Unternehmen, von denen wir gehört haben, versucht auch VectorY, gezielt die mutierte Kopie des Huntingtin-Proteins zu bekämpfen und die normale Kopie zu schonen. Sie konzentrieren sich speziell auf den Teil des Proteins, der durch die CAG-Repeat-Expansion entsteht, die direkt am Anfang des Gens auftritt und als Exon 1 bekannt ist. Dieser Teil kodiert eine lange Kette von Glutaminen, die das Protein klebrig und klumpig machen.
VectorY entwickelt auch eine neue Technik, die als VecTab bekannt ist, ähnlich wie PROTAC, von dem wir bereits gehört haben. Es ist eine weitere Möglichkeit, das schädliche Huntingtin-Protein mit einer „Müllmarke“ zu versehen, die die Zelle anweist, es abzubauen und zu entsorgen. Pavlina teilt Daten mit, die zeigen, dass diese „VecTabs“ die Menge der Huntingtin-Klumpen in den Zellen in einer Schale reduzieren. Sie haben auch Mäuse mit Huntington-Krankheit behandelt und konnten bisher eine Verringerung der Huntingtin-Klumpen sowie eine Verbesserung der Bewegungssymptome feststellen.
Sie arbeiten auch an einer Behandlung für ALS, bei der Viren zum Einsatz kommen, und haben deren Fähigkeit getestet, sich im Gehirn von Mäusen und größeren Tieren wie Schweinen und Primaten auszubreiten. Bisher ist eine gute Ausbreitung zu beobachten, was bedeutet, dass die Behandlung viele Bereiche des Gehirns erreicht. VectorY arbeitet auch an der Verbesserung der Technologien, die erforderlich sind, um ihre Ziele für die Beseitigung durch die Zelle auszurichten, die Medikamente an die richtigen Teile des Gehirns zu bringen und die Medikamente in dem für die Versorgung der Patienten erforderlichen Umfang herzustellen.
MSH3 im Visier
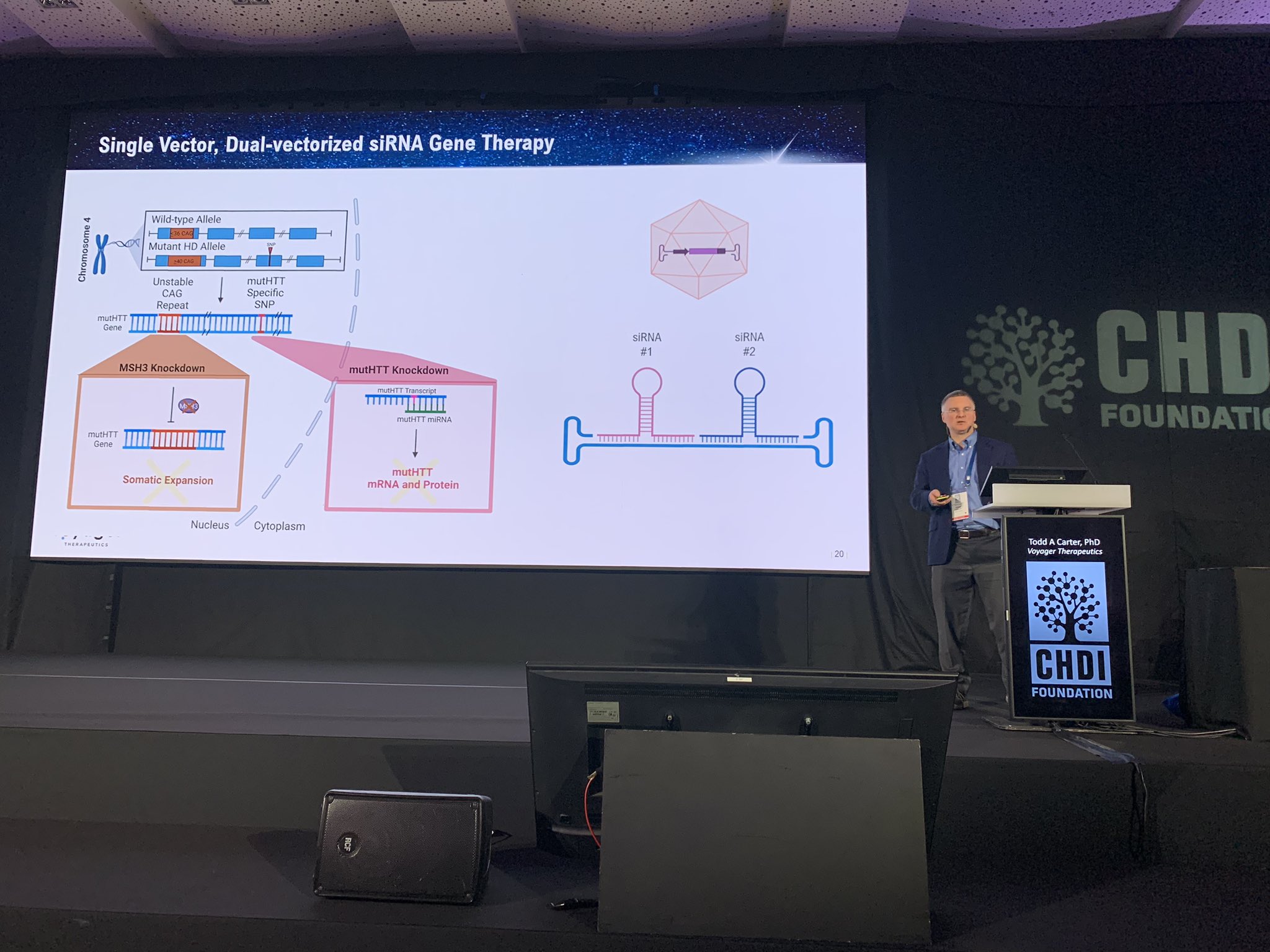
Der letzte Vortrag vor der Mittagspause stammt von Dr. Todd Carter von Voyager Therapeutics – richtig, ein weiteres Unternehmen, das an der Huntington-Krankheit arbeitet, sehr spannend! Voyager arbeitet an MSH3, dem genetischen Modifikator, über den wir gestern schon viel gehört haben. Voyager ist ein „Gentherapie“-Unternehmen, das heißt, es konzentriert sich darauf, Therapien mithilfe harmloser Viruspartikel in die Körperzellen einzubringen. Der besondere Schwerpunkt von Voyager liegt auf einem Virustyp namens AAV, der von Natur aus sehr gut in Gehirnzellen eindringen kann, die das wichtigste Ziel für die HK sind.
Todd beschreibt, dass die neuen Viruspartikel von Voyager, die sie TRACER AAV nennen, eine ganz besondere Fähigkeit haben. Im Gegensatz zu natürlichen AAVs ist dieses künstlich hergestellte Virus in der Lage, in das Gehirn einzudringen, nachdem es in den Blutkreislauf injiziert wurde. Die meisten AAVs werden von der Blut-Hirn-Schranke (BHS) vollständig aufgehalten, einer dichten Versiegelung, die das Gehirn vor schädlichen Dingen wie Viren und anderen toxischen Molekülen schützt, die sich gelegentlich im Blut befinden. Die meisten AAV werden, wenn sie in das Blut injiziert werden, vollständig vom Gehirn ferngehalten.
Mit Hilfe einer ausgeklügelten Technologie hat Voyager AAVs konstruiert, die nach einer einfachen Injektion in das Blut den Weg durch die BHS ins Gehirn finden können. Wenn dies funktioniert, könnte es die Gentherapie bei der HK im Vergleich zu früheren Ansätzen, die auf direkte Injektionen ins Gehirn angewiesen waren, vereinfachen. Im Vergleich zu natürlichen Viren erreichen die neuen AAVs von Voyager einen größeren Teil des Affengehirns, als sie getestet wurden. Dies deutet darauf hin, dass es eine gute Möglichkeit gibt, nützliche Güter in die Gehirne von Menschen mit der HK zu bringen. Ein interessantes Merkmal dieser Technologie ist, dass sie dazu verwendet werden könnte, mehrere Therapeutika gleichzeitig in das Gehirn zu bringen. So könnten zum Beispiel Huntingtin-senkende und MSH3-ausrichtende Medikamente in einer Kombinationsbehandlung für Menschen mit der HK eingesetzt werden.
Biomarker und HK: die Grundsatzrede
Nach einer kurzen Pause sind wir heute Nachmittag mit dem Hauptredner zurück. Der Vortrag wird von Dr. Henrik Zetterberg gehalten, der mit der Universität Göteborg und dem University College London verbunden ist. Im Mittelpunkt seines Vortrags stehen Biomarker für die Huntington-Krankheit, darunter das Neurofilament-Light, auch NfL genannt.
Henrik beginnt mit einem Rückblick auf die Menschen, die Technologie und die Entdeckungen, die uns zur Verwendung von NfL als Biomarker geführt haben – etwas, das wir zuverlässig messen können, um das Fortschreiten von der HK und anderen Hirnerkrankungen zu verfolgen. Die Arbeit von Teams am University College London, darunter auch Prof. Ed Wild von HDBuzz, hat gezeigt, dass es einen Zusammenhang zwischen der NfL-Konzentration und Aspekten der Huntington-Krankheit gibt, z. B. der Länge der CAG-Repeats und dem Zeitpunkt des Auftretens der Symptome. NfL kann als Marker für Hirnschäden bei Verletzungen und Krankheiten verwendet werden; so hat Henrik beispielsweise bei Boxern direkt nach dem Sport erhöhte NfL-Werte nachgewiesen, insbesondere wenn sie viele Treffer einstecken mussten. Der NfL-Spiegel sinkt auch nach erfolgreicher Behandlung von Krankheiten des Nervensystems wie Multipler Sklerose, spinaler Muskelatrophie, HIV und neuerdings auch Formen der Batten-Krankheit und Alzheimer. Forscher können NfL in Bioflüssigkeiten wie Blut und Liquor (die Flüssigkeit, die das Gehirn und das Rückenmark umspült) messen. Bei einigen Krankheiten wie Morbus Huntington und Alzheimer steigt der NfL-Spiegel genau dann an, wenn die ersten Symptome auftreten.
Henriks Labor verwendet NfL auch, um herauszufinden, ob eine Person mit neuen Symptomen an einer psychiatrischen Krankheit wie einer schweren Depression oder Schizophrenie (niedrige NfL) oder an einer neurodegenerativen Krankheit wie der Huntington-Krankheit oder Alzheimer (hohe NfL) leidet. Ein weiterer Bereich, in dem die NfL-Messung nützlich sein könnte, ist die Unterstützung von Ärzten bei der Feststellung, ob eine Person nach einer Vollnarkose, Krebsbehandlung oder Operation neurologische Schäden oder unerwartete Nebenwirkungen erleidet. Neue Methoden machen es immer einfacher, NfL zu messen – anstatt eine Probe der Rückenmarksflüssigkeit zu nehmen und sie für die Analyse sorgfältig aufzubewahren, könnte die Probenentnahme zu Hause mit einem Stich in den Finger erfolgen! Er betrachtet NfL auch aus einigen unerwarteten und ziemlich verrückten Blickwinkeln – er zeigt zum Beispiel, dass die Stützzellen des Gehirns NfL „fressen“, dass es bei Bären ansteigt, wenn sie Winterschlaf halten, oder dass es bei Astronauten, die ins All fliegen, zunimmt! Insgesamt unterstreicht Henrik, dass NfL nützlich sein kann, um den Beginn der Krankheit zu messen, um die Sicherheit eines Medikaments oder eines Verfahrens zu verstehen und um andere Faktoren zu beobachten, die die Symptome der Huntington-Krankheit beeinflussen, wie Alter und genetische Variationen.
Das war’s für Tag 2! Wir melden uns morgen früh zurück, um über den dritten und letzten Tag der HDTC2023 zu berichten! Vergessen Sie nicht, den Live-Updates für den Rest der Konferenz auf Twitter mit dem Hashtag #HDTC2023 zu folgen.
For more information about our disclosure policy see our FAQ…


