Huntington's Disease Therapeutics Conference 2024 - Tag 1
Lesen Sie die neuesten Forschungsergebnisse von Tag 1 der 2024 HD Therapeutics Conference #HDTC2024
Bearbeitet von Dr Rachel Harding, Dr Sarah Hernandez und Dr Leora Fox 6. März 2024 Von Dr Leora Fox, Dr Rachel Harding und Dr Sarah Hernandez Übersetzt von Rebecca Ursprünglich veröffentlicht am 5. März 2024
Das HDBuzz-Team traf sich kürzlich in Palm Springs, Kalifornien, zusammen mit hunderten von anderen Wissenschaftlern aus der ganzen Welt zur 19. jährlichen HD Therapeutics Conference, die von der Huntington-Forschungsstiftung CHDI veranstaltet wurde. Von Dienstag, dem 27. Februar, bis Donnerstag, dem 29. Februar, haben wir dutzende wissenschaftlicher Vorträge von internationalen Experten auf dem Gebiet der Huntington-Forschung live getwittert, von Wissenschaftlern aus der Praxis bis hin zu Klinikärzten. Wir haben unsere Tweets der gesamten Konferenz zusammengefasst, beginnend mit Tag 1:
Huntingtin Hausaufgaben: Einem alten Dogma neue Tricks beibringen
Die erste Sitzung der Konferenz konzentrierte sich auf Huntingtin und die Auslöser der Huntington-Krankheit. Den Auftakt machte Gill Bates, die einen Überblick über die genetischen Grundlagen der Huntington-Krankheit gab. Demnach entscheidet die Länge der CAG-Wiederholungen im Huntingtin-Gen darüber, ob Menschen an Huntington erkranken. In jüngerer Zeit wurde eine zusätzliche Zunahme der CAG-Anzahl über die Zeit in einigen Gehirnzellen, die so genannte somatische Expansion, als Ursache der Krankheit identifiziert.

Es gibt noch viele unbeantwortete Fragen darüber, wie genau die CAG-Expansion zum Absterben von Gehirnzellen führt. In dieser Sitzung wurde ein breites Spektrum von Ansätzen auf epigenetischer, RNA- und Proteinebene behandelt.
Karine Merienne: DNA-Marker im Striatum
Die erste Rednerin der Konferenz war Karine Merienne von der Universität Straßburg, die uns über Veränderungen bestimmter Marker bei Huntington im Zusammenhang mit dem Altern informierte. Karine erinnerte uns daran, dass es immer noch ein Rätsel ist, warum die Nervenzellen des Striatums so anfällig für die CAG-Expansion im Huntingtin-Gen sind. Eine Hypothese, die sie untersucht, sind Veränderungen in der Gen-An- und Abschaltung.
Karines Forschung befasst sich also damit, wie sogenannte epigenetische Veränderungen bei Huntington auftreten. Dabei handelt es sich nicht um Veränderungen des DNA-Codes selbst, sondern um bestimmte Marker, die die Art und Weise beeinflussen, wie die DNA verpackt ist. Dies wiederum definiert, welche Gene ein- oder ausgeschaltet werden, was sich auf die Eigenschaften der Zellen auswirkt und schlussendlich eine Nervenzelle zu einer Nervenzelle oder eine Hautzelle zu einer Hautzelle macht.
Die epigenetischen Marker verändern sich mit dem Alter bei allen Menschen, nicht nur bei Menschen mit Huntington. Karines Team fand heraus, dass bestimmte epigenetische Marker in Mausmodellen der Huntington-Krankheit weiter verändert sind. Mithilfe modernster Technologien konnten sie die Veränderungen der Marker auf der Ebene einzelner Gehirnzellen einer Maus untersuchen. Sie sahen, dass Nervenzellen aus dem Striatum, der anfälligen Hirnregion bei Huntington, eine wichtige epigenetische Markierung fehlte.
Dies gibt uns Aufschluss darüber, warum die Zellen im Striatum bei Menschen mit Huntington eher erkranken können. Wenn wir diese epigenetischen Markierungen reparieren können, könnten wir die Zellen vielleicht wieder gesund machen? Wir werden sehen; es gibt eine Menge kluger Leute, die daran arbeiten!
Yinsheng Wang: Chemische Markierungen richten Unheil an
Der nächste Vortrag des Vormittags kam von Yinsheng Wang, der an der University of California, Riverside, arbeitet. Yinsheng untersucht, wie genetische Botenmoleküle bei Huntington und anderen CAG-Krankheiten durch chemische Markierungen verändert werden.
Die sich wiederholenden CAGs in der Botschaft des Huntingtin-Gens können mit zusätzlichen Molekülen "markiert” werden. Im Verlauf der Huntington-Krankheit können die zusätzlichen Markierungen Proteine in der Zelle in unangemessener Weise rekrutieren, so dass sie aufgesaugt werden und ihre normalen Aufgaben nicht mehr erfüllen können. Interessanterweise scheinen diese Veränderungen an den Markierungen des Huntingtin-Botschaftsmoleküls bei HD-Mäusen am häufigsten im Striatum aufzutreten. Könnte dies ein weiterer Grund sein, warum diese Gehirnzellen am häufigsten erkranken?
Spezielle molekulare Maschinen fügen diese Markierungen am Huntingtin-Molekül hinzu oder entfernen sie. Yinsheng und seine Kollegen fanden heraus, welche dieser Maschinen für die Veränderungen verantwortlich war, die sie messen konnten. Wenn sie die Maschine ausschalteten, kehrten die Markierungen des Nachrichtenmoleküls in den Normalzustand zurück.
Sie fanden auch heraus, dass Veränderungen der molekularen Markierungen die Fähigkeit der Huntingtin-Botschaft verändern, sich an ein Protein namens TDP-43 zu heften, das bei anderen neurodegenerativen Erkrankungen eine Rolle spielt. (Wie Huntingtin kann auch TDP-43 Klumpen bilden.) Huntingtin kann zusammen mit seinen CAG-Wiederholungen und Tags die Bildung dieser Klumpen beeinflussen. Die Daten dieses Teams legen nahe, dass zusätzliche Wiederholungen auf dem Huntingtin-Botenmolekül zur Verklumpung von TDP-43 führen.
Yinsheng erklärt eine weitere Möglichkeit, wie chemische Markierungen auf dem Huntingtin-Botenmolekül in der Zelle Schaden anrichten können: indem sie das Molekül aus dem Gleichgewicht bringen und toxische Proteine bilden, die es eigentlich nicht kodieren sollte. Wenn wir die Art und Weise, wie es von diesen molekularen Maschinen markiert wird, wiederherstellen können, werden die Gehirnzellen vielleicht weniger krank. Dies ist ein interessanter neuer Weg für die Arzneimittelforschung auf dem Gebiet der Huntington-Krankheit.
Jeff Carroll: Wie tief sollten wir gehen?
Wir haben auch von Jeff Carroll von HDBuzz selbst gehört. Jeffs Labor, das an der University of Washington angesiedelt ist, hat sich mit der Untersuchung der HTT-Senkung in Mausmodellen der Huntington-Krankheit beschäftigt. Jeffs Labor fragt sich, was es tun kann, um die klinischen Huntingtin-Senkungsstrategien zu beschleunigen und zu verbessern. Eine wichtige Frage ist, wie stark Huntingtin reduziert werden kann und in welchen Zelltypen, um die Symptome von Huntington ohne negative Auswirkungen zu verbessern.
Die Schlüsselfragen, die Jeffs Team zu beantworten versucht, lauten: Wie niedrig ist die Huntingtin-Senkung, und wie niedrig muss sie sein, um eine positive Wirkung zu erzielen? Experimente an Mäusen haben gezeigt, dass eine zu niedrige Dosis möglicherweise nicht sehr gut ist. Eines der Projekte, an denen Jeffs Labor arbeitet, befasst sich mit der Huntingtin-Senkung bei erwachsenen Mäusen. Dies entspricht dem, was wir in der Klinik tun, indem wir erwachsenen Menschen mit Huntington verschiedene Arten von Medikamenten verabreichen, um den Huntingtin-Proteinspiegel zu senken.
Jeffs Labor hat gezeigt, dass es nicht sicher ist, Huntingtin im Gehirn von Mäusen vollständig zu entfernen - sie hatten buchstäblich Löcher in ihren Gehirnen! Natürlich ist die vollständige Entfernung von Huntingtin in menschlichen Gehirnen nicht das Ziel klinischer Studien. Der Trick besteht wahrscheinlich darin, das richtige Gleichgewicht zu finden. Jeff betont noch einmal, dass dies nicht bedeutet, dass eine Huntingtin-Senkung per se eine schlechte Idee ist, wir müssen nur herausfinden, wie tief wir gehen können.
Aus genetischen Studien wissen wir, dass 50 % (auf die die meisten klinischen Studien abzielen) bei Menschen und Tiermodellen der Huntington-Krankheit in Ordnung zu sein scheinen, aber vielleicht ist ein Wert darunter keine gute Idee. Eine interessante Beobachtung, die Jeffs Gruppe gemacht hat, ist, dass die Senkung von Huntingtin mit ASOs bei Mäusen die somatische Instabilität, also die Ausdehnung der CAG-Wiederholung in einigen Zellen, zu verändern scheint. Dies scheint in der Leber bei sehr hohen ASO-Dosen zu geschehen. Herauszufinden, warum dies der Fall ist, ist sehr kompliziert!
Noch wichtiger ist die Frage, ob die klinischen Ansätze, bei denen geringere Mengen von ASO verwendet werden, dasselbe bewirken? Es scheint nicht so zu sein. Aber es ist wahrscheinlich etwas, das die Wissenschaftler in Zukunft im Auge behalten sollten.
„Die Entdeckungen auf dem Gebiet der somatischen Instabilität wären ohne das Engagement der Huntington-Familien und ihre Bereitschaft, an der Forschung teilzunehmen, nicht möglich gewesen. “
Als Nächstes untersuchte Jeffs Team selektive Senkungsansätze - Therapien, die nur auf das toxische Huntingtin abzielen und die regulären Huntingtin-Spiegel unangetastet lassen. Auch hier zeigte sich, dass die somatische Instabilität durch diese Behandlungen blockiert zu werden schien - dies könnte eine coole Doppeltherapie zum Preis von einer sein!
Insgesamt hilft uns Jeffs Arbeit, besser zu verstehen, was Huntingtin-Senkung auf molekularer Ebene bedeutet, was uns helfen wird, besser zu verstehen, was in den aktuellen klinischen Studien passiert, und was wir zusätzlich bedenken müssen, um diesem Ansatz die beste Chance zu geben.
Ileana Cristea: Huntingtin und seine Tanzpartner
Wir sind zurück und als Nächste ist Ileana Cristea dran, die eine Forschungsgruppe an der Princeton University leitet. Sie untersucht das Huntingtin-Protein und die anderen Proteine, mit denen es in den Zellen gerne zusammen ist, und wie sich diese Beziehungen bei Huntington verändern. Diese Arbeit fällt in den Bereich der “Omics”-Forschung, bei der Forscher Veränderungen von Proteinen und deren Interaktion in vielen Zellen, Geweben und Gehirnbereichen untersuchen. Es gibt eine enorme Zusammenarbeit!
Ileanas Vortrag setzt das Thema fort, herauszufinden, warum einige Zellen bei Huntington krank werden, während andere scheinbar in Ordnung sind. Ihr Labor untersucht die Orte, an denen sich verschiedene Proteine befinden und welche davon zusammenhängen. Sie versuchen herauszufinden, was die Krankheit auslöst und welche Folgen die Senkung des Huntingtin-Spiegels durch Medikamente hat. Zu diesem Zweck untersuchen sie, welche Proteine in Gegenwart und Abwesenheit von Huntingtin interagieren.
Sie fanden heraus, dass in Zellen von Mäusen, denen das Huntingtin-Protein fehlt, die Konzentrationen aller möglichen Proteine verändert waren und auch, welche Proteine zusammenhängen. Die größten Veränderungen traten bei Proteinen auf, die an der Energieerzeugung und der DNA-Reparatur beteiligt sind. Der nächste Schritt bestand darin, zu verstehen, wie diese Veränderungen zu der Krankheit führen, und so konzentrierten sich die Forscher auf das Striatum von Mäusen mit Huntington, da diese Gehirnregion bei Huntington am stärksten betroffen ist.
Sie stellten eine Liste von Proteinen zusammen, die an bestimmten Zellfunktionen beteiligt sind und uns Hinweise darauf geben könnten, was bei Huntington schief läuft. Nachdem sie sich einen Überblick über die Netzwerke verschafft hatten, die miteinander interagieren, bestätigten sie einige ihrer “Treffer” in Zusammenarbeit mit Wissenschaftlern, die an anderen Modellen und Techniken arbeiten, z. B. an Zellen und Fruchtfliegen. In verschiedenen Zelltypen sind unterschiedliche Proteinknospen von Huntingtin verändert, was wiederum erklären könnte, warum verschiedene Zellen bei der Huntington-Krankheit auf unterschiedliche Weise betroffen sind.
Ileanas Team kann nicht nur herausfinden, mit welchen Proteinen Huntingtin zusammenhängt, sondern auch, durch welche Oberflächen sie alle zusammenhalten, was ein sehr detailliertes molekulares Bild der Vorgänge bei Huntington ergibt. Auch wenn diese Art von Studie etwas grobschlächtig erscheint, ist sie doch sehr wichtig, um zu verstehen, was bei Huntington genau schief läuft. Sie hilft uns auch dabei, neue Gene und Proteine zu identifizieren, die gute Ziele für die künftige Entdeckung von Medikamenten sein könnten.
Tony Reiner: Muster von Huntingtin-Klumpen
Der letzte Vortrag des Vormittags kam von Tony Reiner, der am University of Tennessee Health Science Center arbeitet. Sein Team hat untersucht, wo die Krankheitsform des Huntingtin-Proteins in den Gehirnen von Menschen und Mäusen mit Huntington-Krankheit vorkommt.
Tony erinnerte uns zunächst an die spezifischen Teile des Gehirns, die bei Huntington am anfälligsten sind. Das Striatum, das sich im Zentrum des Gehirns befindet, ist eine der am stärksten betroffenen Hirnregionen, aber auch Nervenzellen im Kortex und Thalamus sind betroffen. Die Hirnregionen, in denen viel Huntingtin-Protein gebildet wird, sind bei Huntington nicht unbedingt am stärksten betroffen. Regelmäßiges Huntingtin kommt eigentlich überall vor, so dass dies nicht zu erklären scheint, warum die Zellen im Striatum so anfällig sind.
Huntingtin-Proteine gibt es in vielen verschiedenen Varianten - expandiert, fragmentiert, verklumpt und andere. Tonys Gruppe verwendet Antikörper als Hilfsmittel, um die verschiedenen Formen des Huntingtin-Proteins im Gehirn sichtbar zu machen. Zunächst untersuchten sie Gehirne von Huntington-Mäusen und versuchten, diese mit Gewebe von Menschen mit Huntington abzugleichen, die ihre Gehirne nach ihrem Tod großzügig für die Forschung gespendet hatten. Dieser selbstlose Akt war entscheidend für die Gewinnung von Daten, die uns Aufschluss darüber geben, was mit der Huntington-Krankheit in menschlichen Gehirnen vor sich geht.
Wenn Sie daran interessiert sind, können Sie mehr über Gehirnspenden beim Brain Donor Project (https://braindonorproject.org/), bei HDSA, HSC, bei HD-Organisationen in Ihrem Heimatland und bei lokalen akademischen Einrichtungen erfahren.
Wir können viele Veränderungen in den Gehirnzellen im Laufe der Zeit messen, aber es ist immer noch nicht ganz klar, welche Veränderungen tatsächlich dazu führen, dass die Zellen krank werden. Tonys Arbeit zeigt, dass erhöhte Proteinklumpen und andere Messungen nicht immer mit den Zellen übereinstimmen, von denen wir wissen, dass sie krank werden. Die Arbeiten von Tonys Labor und anderen befassen sich mit diesen Messungen auf der Ebene der verschiedenen Zelltypen, die uns eines Tages helfen könnten, Ursache und Wirkung besser zu verstehen.
Zielgerichtete DNA-Reparaturmechanismen zur Beeinflussung der somatischen Instabilität
Sitzung 2 der Konferenz befasste sich mit Möglichkeiten zur Bekämpfung der Ausbreitung von CAG-Wiederholungen. Dies geschieht in einigen Zellen, wenn sich die HD-Symptome verschlimmern. Viele neue Erkenntnisse deuten darauf hin, dass die Verlängerung der CAG-Wiederholungen ein wichtiger Faktor für den Zellverlust im Striatum ist und das Auftreten von Symptomen verfrüht. Anhand des von Tausenden von Menschen mit Huntington gespendeten Blutes konnten Wissenschaftler große genetische Studien (so genannte GWAS) durchführen, um weitere Gene zu bestimmen, die das Auftreten von Huntington beeinflussen. Insbesondere sind viele dieser Gene an der so genannten DNA-Reparatur beteiligt.
Die DNA-Reparatur ist ein Prozess, bei dem kleine molekulare Maschinen Fehler oder Veränderungen im Rechtschreibcode der DNA reparieren. Eine dieser Veränderungen, die bei der Huntington-Krankheit auftreten, ist die Zunahme der CAG-Wiederholung. Manche Menschen haben DNA-Reparaturmaschinen, die sehr gut in der Lage sind, Fehler zu erkennen, andere wiederum haben Maschinen, die nicht so gut sind. Wenn die DNA-Reparaturmaschinerie versagt, kann sich der CAG-Repeat in einigen Zellen mit der Zeit verlängern.
Viele Huntington-Wissenschaftler glauben nun, dass es möglich sein könnte, die Verlängerung der CAG-Wiederholungen in den anfälligen Gehirnzellen zu verlangsamen, indem man gezielt in die DNA-Reparaturgene eingreift und so den Ausbruch oder die Verschlimmerung der Huntington-Symptome hinauszögert. Immer mehr Wissenschaftler und Unternehmen suchen, bestätigen und testen verschiedene Akteure innerhalb der DNA-Reparaturmaschinerie, um herauszufinden, was schief läuft, wenn die CAG-Wiederholungen länger werden, und um zu versuchen, dies zu verhindern.
Wir werden mit vielen Akronymen und Namen von Proteinen um uns werfen, von denen bekannt ist, dass sie am DNA-Reparaturprozess beteiligt sind. Diese Proteine arbeiten zusammen, um die DNA auf unterschiedliche Weise zu reparieren, und können bei Huntington gestört werden. Wissenschaftler entwickeln derzeit genetische Medikamente, um ihre Konzentration zu erhöhen oder zu verringern und die CAG-Expansion zu stoppen.
Maren Thomsen: Die Form der DNA-Reparaturmaschinen
Die erste Rednerin des Nachmittags war eine Strukturbiologin, Maren Thomsen von der Firma Proteros Biostructures. Sie untersucht die Form eines Proteins namens MutSꞵ, das an der DNA-Reparatur beteiligt ist. Mit Hilfe spezieller Mikroskope können sie genau sehen, wie das Protein im 3D-Raum organisiert ist, was den Wissenschaftlern helfen kann, herauszufinden, wie es funktioniert.
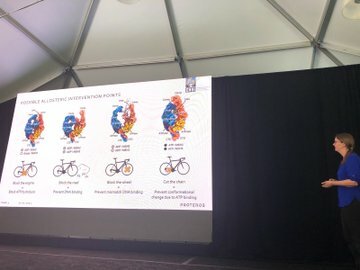
Im Idealfall würden wir die Aktivität von MutSꞵ gerne stoppen, und es gibt verschiedene Möglichkeiten, dies zu tun. Maren verwendet die Analogie zu dem Versuch, die Bewegung eines Fahrrads zu stoppen: Man könnte die Pedale anhalten, eine Barrikade davor stellen oder das Rad am Drehen hindern. Wenn sie die Details der MutSꞵ-Struktur kennen, können sie sich verschiedene Möglichkeiten ausdenken, um die Bewegung zu stoppen.
Mit kühlen Mikroskopen können Maren und ihr Team genau herausfinden, wo sich jedes Atom des Proteins befindet und wie es sich verändert, wenn MutSꞵ an der DNA entlanggleitet und sie repariert. Mit dieser hohen Informationsauflösung können sie ein sehr detailliertes Modell der Funktionsweise dieser molekularen Maschine erstellen. Sie kann sich wirklich bewegen, indem sie die DNA wie eine Klammer umgreift und öffnet! Wenn Marens Team Änderungen an der MutSꞵ-Maschine vornimmt, verändert sich ihr Griff und ihre Bewegung, und sie lernen mehr darüber, welche Teile des Proteins an anderen Akteuren im DNA-Reparaturprozess haften.
Maren untersucht auch ein Protein namens FAN1 und seine “Tanzpartner”. FAN1 ist ebenfalls an der DNA-Reparatur beteiligt, und ihre Gruppe konnte es auf neue Weise sichtbar machen, mit dem Ziel, es für die Entwicklung von Medikamenten nutzbar zu machen. Mit diesen detaillierten Einblicken in das Zusammenspiel all dieser Moleküle können wir beginnen zu verstehen, warum bestimmte Mutationen, die in GWAS gefunden wurden, das Alter des Auftretens von Symptomen bei Huntington verzögern oder beschleunigen können.
Strukturbiologische Techniken beleuchten die Form und Bewegung wichtiger Moleküle, so dass wir besser verstehen können, wo und wie wir in die fehlerhafte Biologie der Huntington-Krankheit eingreifen und Medikamente entwickeln können, die genau auf Proteine wie MutSꞵ abzielen.
Wei Yang: MutSꞵ und lange CAG-Wiederholungen
Als nächstes hörten wir von einem anderen Strukturbiologen, Wei Yang, der an den National Institutes of Health arbeitet und ebenfalls MutSꞵ untersucht. Die MutSꞵ-Molekularmaschine wirkt auf alle Arten von sich wiederholenden DNA-Sequenzen, nicht nur auf CAG-Wiederholungen. Wei’s Team hat mit Hilfe strukturbiologischer Ansätze herausgefunden, wie genau MutSꞵ an diese sich wiederholenden DNA-Buchstaben bindet.
Ein interessantes Rätsel ist die Frage, warum es einen Schwellenwert von CAGs gibt, bei dem sich die Wiederholungen mit der Zeit weiter ausdehnen. Um dies zu verstehen, sind saubere Experimente erforderlich, bei denen die CAG-Wiederholungen in der DNA und ihre Bindung an MutSꞵ untersucht werden. Wei und ihr Team fanden heraus, dass MutSꞵ viel lieber an längere CAG-Wiederholungen bindet als an kürzere. Wenn die CAG-Strecke lang genug ist, bindet sogar mehr als ein MutSꞵ-Molekül an die CAG-DNA.
Wenn sie sich die CAG-DNA ansehen, die an MutSꞵ klebt, sehen sie, dass MutSꞵ die CAG-Wiederholungs-DNA so verformt, dass sie wie nicht-wiederholende DNA aussieht. Es funktioniert wie ein Schraubstock, um die DNA in diese andere Form zu biegen. Es überrascht nicht, dass dies eine Menge Energie erfordert. Aber was bedeutet das alles für HD? Nun, wenn sich die CAGs oft genug wiederholen, wie es bei Menschen mit HD der Fall ist, binden sich immer mehr MutSꞵ-Moleküle an. Wei glaubt, dass dies ungewollt die CAG-Expansion fördern könnte.
Strukturbiologische Studien helfen uns, Erkenntnisse von Menschen zu bestätigen, die die Bedeutung der DNA-Reparatur bei Huntington gezeigt haben. Wir erfahren mehr über die Gene und den Mechanismus, die an der somatischen Instabilität beteiligt sind, und darüber, wie diese mit dem Auftreten der Symptome zusammenhängen könnte. Mit diesem Wissen ausgestattet, können Medikamentenjäger Wege finden, MutSꞵ davon abzuhalten, Fehler zu machen, die CAGs verlängern, mit dem Ziel, HD zu verlangsamen oder zu stoppen.
Tatsächlich haben Wei und ihr Team eine Verbindung identifiziert, die die Art und Weise verändert, wie MutSꞵ an der CAG-DNA haftet. Obwohl dieses Molekül wahrscheinlich kein Medikament sein wird, könnte es ein hilfreicher Ausgangspunkt für die Suche nach Medikamenten sein.
Sarah Tabrizi: Erforschung der DNA-Reparatur in menschlichen Zellen
Als Nächste war die legendäre Sarah Tabrizi an der Reihe, eine Ärztin und Wissenschaftlerin vom University College London, die in der Grundlagenforschung und der klinischen HD-Forschung tätig ist. Sarah Tabrizi verwendet menschliche Zellen, die in einer Schale gezüchtet werden, um viele der Gene, die als wichtig für die DNA-Reparatur und die CAG-Repeat-Expansion identifiziert wurden, weiter zu testen. Es gibt eine Vielzahl von DNA-Reparaturproteinen, die als gute Ziele für Therapien in Frage kommen.
Sarah und ihr Team setzen gentechnische Verfahren wie CRISPR ein, um die Konzentration von DNA-Reparaturproteinen zu senken, die bei Huntington gestört sind. Anschließend untersuchen sie, wie sich dies auf die Konzentrationen anderer Gene auswirkt, um die Beziehungen zwischen den DNA-Reparaturmechanismen zu ergründen. Nachdem sie die Konzentrationen verschiedener DNA-Reparaturproteine verändert hatten, untersuchte Sarahs Team, wie sich dies auf die Expansion der CAG-Wiederholungen auswirkt. Sie nahmen die Gene MSH2 und MSH3 ins Visier. Die Senkung dieser (und anderer) Gene reduzierte das Ausmaß der somatischen Expansion.
Bei Stammzellen, die dazu gebracht wurden, sich zu Gehirnzellen zu entwickeln, führte die Senkung eines bestimmten DNA-Reparaturgens namens MLH1 zu einer Verringerung der somatischen Expansion um 78 % - wow! Sie erforscht auch andere Ziele, darunter ein Gen namens MSH3, das sie als “ideales therapeutisches Ziel” bezeichnet. Ihre Arbeit hebt zwei Reparaturproteine namens MLH1 und PMS1 als potenziell interessante Arzneimittelziele hervor. Die Arbeit an Targets jenseits des MutSꞵ-Komplexes könnte sehr nützlich sein, um unsere Chancen zu erhöhen, wirksame Medikamente zu finden.
Nichtsdestotrotz bekräftigt Sarah, dass MSH3 ihr bevorzugter Angriffspunkt für Medikamente ist, da das Ausschalten dieses Proteins die Ausbreitung der CAG-Wiederholungen zu verlangsamen scheint. Außerdem scheint die Verarmung dieses Proteins keine allzu großen Nebenwirkungen zu haben, zumindest in Modellen. Sarahs Labor verwendet ASOs, um die MSH3-Konzentration zu senken, dieselbe Art von Medikamenten, die einige Unternehmen (wie Roche) zur Senkung von Huntingtin einsetzen. Als sie den MSH3-Spiegel senkten, verlangsamte dies die somatische Expansion. Als sie MSH3 vollständig entfernten, wurden die CAG-Wiederholungen kleiner. Andere DNA-Reparaturproteine waren davon nicht betroffen, was eine gute Nachricht für die Entwicklung von MSH3-Medikamenten ist.
Fast alle diese Arbeiten wurden an Nervenzellen in einer Schale durchgeführt, die aus einer Blutprobe hergestellt worden war, die Sarah großzügig von einem jungen Patienten gespendet bekam, den sie vor dessen Tod behandelte. Diese und viele andere Entdeckungen auf dem Gebiet der somatischen Instabilität wären ohne das Engagement der Familien von Huntington-Patienten und ihre Bereitschaft, an der Forschung teilzunehmen, nicht möglich gewesen. Sarahs Team setzt diese Arbeit in einem Mausmodell fort, um zu sehen, wie ihre MSH3-ASOs in einem komplexeren System wirken. Bleiben Sie mit uns dran!
Ricardo Mouro Pinto: Erforschung von DNA-Reparaturgenen als potenzielle Angriffspunkte
Ricardo Mouro Pinto ist am Massachusetts General Hospital und der Harvard Medical School tätig. Sein Team untersucht auch die somatische Expansion. Bei Patienten mit erhöhter somatischer Instabilität treten die HD-Symptome früher auf. Die Gene, die das Auftreten der Symptome beeinflussen, werden als genetische Modifikatoren bezeichnet. Ricardo und andere testen die Theorie, dass eine Veränderung der Werte dieser Modifikatoren den Ausbruch der Huntington-Krankheit verzögern oder stoppen kann.
Ricardo setzt CRISPR ein, um die Konzentration dieser Modifikatoren in Mäusen zu verändern, die als Modell für Huntington dienen. Er hat 60 verschiedene Gene bei Mäusen untersucht - das ist eine Menge Arbeit! Das Ergebnis dieser Arbeit ist, dass DNA-Reparaturgene einen großen Einfluss auf die Länge der CAG-Wiederholungen haben. Dies bestätigt, was viele andere Forscher auf diesem Gebiet festgestellt haben. Jedes Mal, wenn Ergebnisse in verschiedenen Labors auf der ganzen Welt repliziert werden, stärkt dies das Vertrauen des Fachgebiets in diese Daten.
Anschließend wandte er sich menschlichen Zellen zu, die in einer Schale gezüchtet wurden, um die eigenen Daten und die der anderen zu bestätigen. Sie fanden heraus, dass eine Senkung von MSH3 die Expansionsrate verlangsamt und eine Senkung von FAN1 sie erhöht. Sie fanden auch heraus, dass eine Verringerung der Werte von MLH3 und PMS1 die Ausbreitung stoppt. Ricardo arbeitet auch daran, diese Modifizierungsziele bei anderen Krankheiten zu überprüfen. HD ist nicht die einzige Krankheit, die von somatischer Expansion betroffen ist. Daher testet er die Ziele, die er bei der Huntington-Krankheit identifiziert hat, bei Mäusen, die andere Krankheiten wie die Frederich-Ataxie modellieren.
Wenn man auf ein und dasselbe Protein abzielt, das an mehreren Krankheiten beteiligt ist, profitieren nicht nur mehr Menschen davon, sondern es könnte auch die Aufnahme von Studien und die Entwicklung von Medikamenten beschleunigen. Aber bevor wir uns zu früh freuen, müssen diese Zielmoleküle noch weiter getestet werden, um sicherzustellen, dass sie die gewünschte Wirkung haben! Ein Punkt, dessen sich die Forscher bewusst sein müssen, ist, dass DNA-Reparaturgene auch bei Krebs eine Rolle spielen. Ricardo berücksichtigt dies und wählt potenzielle Wirkstoffziele aus, bei denen die Wahrscheinlichkeit, dass sie bei Menschen zu Krebs führen, am geringsten ist.
Ein Ziel, an dem Ricardos Team besonders interessiert ist, heißt MLH3. Sie haben einige detaillierte Studien durchgeführt, um herauszufinden, welcher Teil des MLH3-Gens für die somatische Expansion bei Huntington verantwortlich ist. Wenn die Forscher genau wissen, welcher Teil des Gens für die Beeinflussung der CAG-Länge verantwortlich ist, wissen sie, auf welche Stelle sie bei der Entwicklung eines Medikaments gegen MLH3 abzielen müssen.
Mit Hilfe cooler gentechnischer Verfahren ist Ricardo in der Lage, Zellen herzustellen, die eine Version von MLH3 produzieren, die den Teil des Codes ausschließt, der zur CAG-Wiederholungsexpansion führt. Auf diese Weise konnte er die CAG-Expansion unterdrücken. Jetzt arbeitet er daran, mit CRISPR einen einzigen Buchstaben in der Sequenz von MLH3 zu verändern. Dies ist ein präziser Ansatz, der MLH3 daran hindert, die CAG-Zahl zu erhöhen, während die übrigen Funktionen von MLH3 erhalten bleiben.
Dies ist wichtig, weil Proteine in Zellen viele verschiedene Funktionen haben. Wenn man auf eine einzige Funktion abzielt, verringert sich die Wahrscheinlichkeit unbeabsichtigter Folgen. Etwas, das für die Entwicklung von Medikamenten entscheidend ist! Ricardos nächste Schritte sind die Verwendung seiner neuen CRISPR-Ansätze zur Veränderung von MLH3 in Mäusen und menschlichen Zellen in einer Schale. Dafür erhielt Ricardo kürzlich einen Zuschuss in Höhe von 1.000.000 $ von der Hereditary Disease Foundation!.
Karen Usdin: somatische Expansion bei anderen Krankheiten
Karen Usdin von den National Institutes of Health sprach über die Arbeit ihres Teams, das sich mit der somatischen Expansion bei verschiedenen Arten von Krankheiten befasst, die durch DNA-Wiederholungen verursacht werden, abgesehen von HD. Es gibt viele Krankheiten, die durch sich wiederholende DNA-Sequenzen verursacht werden. Karens Team konzentriert sich in erster Linie auf eine dieser Krankheiten namens Fragile X, die durch ein sich wiederholendes CGG verursacht wird. Doch jetzt beginnt sie, sich auch mit der Huntington-Krankheit zu befassen. Juhu!
Bei Fragile X gibt es auch eine somatische Expansion, die durch DNA-Reparaturgene gesteuert wird. Karen hat Mäuse als Modell für Fragile X verwendet, um herauszufinden, welche DNA-Reparaturgene für diesen Prozess bei Fragile X wichtig sind.
Ihr Labor eliminierte einen Teil des MutL-Komplexes, genannt PMS2. Die Senkung des PMS2-Spiegels stoppte die Ausbreitung von Wiederholungen in menschlichen Zellen und Mäusen mit anderen genetischen Krankheiten. Ähnliche Ergebnisse erzielte sie mit einem anderen Teil des MutL-Komplexes namens PMS1. Eine Senkung des PMS1-Spiegels verringerte die Expansionen bei Fragile X. Zusammen mit den Daten anderer Krankheiten deutet dies darauf hin, dass PMS1 eine Rolle bei der Expansion von Wiederholungskrankheiten spielt.
Jetzt kommt Karen zu den guten Dingen - ihrer Arbeit über Huntington! Sie stellte ein Mausmodell her, das sowohl Gene für die Huntington-Krankheit als auch für Fragile X aufwies. Mit dieser Maus konnte sie die Repeat-Expansion in beiden Genen gleichzeitig untersuchen. Sie wollte wissen, ob die Expansion des einen Gens die Expansion des anderen Gens beeinflusst. Einfach ausgedrückt - nein. Die Expansionen des HD-Gens hatten keinen Einfluss auf das Gen für Fragiles X und umgekehrt.
Sie vermutet, dass die Expansionen vom Gleichgewicht zwischen verschiedenen Arten von DNA-Reparaturmaschinen in verschiedenen Zellen abhängen. Einige der Ideen, die sie vorbringt, sind reine Theorie, aber sie begrüßte es, wenn andere Wissenschaftler sich bei einem Getränk darüber austauschten! Konferenzen wie diese sind ein fantastischer Ort, um Ideen auszutauschen.
Rgenta Therapeutics: orale Medikamente für die DNA-Reparatur
Der letzte Vortrag des Tages kam von Travis Wager von Rgenta Therapeutics. Travis erzählte uns von den Medikamenten, die sein Team entwickelt und die oral eingenommen werden können und auf den Modifikator PMS1 abzielen, um die somatische Expansion in klinischen Studien am Menschen zu verlangsamen.
Rgenta hat die letzten vier Jahre damit verbracht, darüber nachzudenken, wie sie Targets angehen können, die traditionell als “unbehandelbar” galten. Andere Unternehmen haben in der Vergangenheit erfolglos versucht, auf Gene zu zielen, die die somatische Expansion kontrollieren, wie PMS1 und MSH3. Die Medikamente von Rgenta wirken wie Klebstoffe, die eine stärkere Verbindung zwischen krankheitsverursachenden RNA-Botschaften und den Proteinen, die an sie binden, herstellen, um die Herstellung von Proteinen zu verändern oder eine fehlerhafte Botschaft oder ein fehlerhaftes Protein zu beseitigen.
Travis wies auf die verschiedenen Krankheiten hin, gegen die sie mit ihren Medikamenten gegen Gene, die die somatische Expansion kontrollieren, vorgehen wollen. Dazu gehören Huntington, myotonische Dystrophie, Fragiles X und Fredreich-Ataxie: allesamt Krankheiten mit Wiederholungsexpansion. Das Interesse von Rgenta an der Huntington-Krankheit beruht auf der Verfügbarkeit riesiger Datenmengen von Menschen und Tieren, was ein Beweis für die Zusammenarbeit und das Engagement von Wissenschaftlern und Huntington-Familien ist. Der Bereich der Huntington-Krankheit zieht aus diesem Grund viele Unternehmen an.
Rgenta hat sich auf PMS1 konzentriert, weil höhere PMS1-Werte bei Menschen mit einem früheren Auftreten der Huntington-Symptome in Verbindung gebracht werden. Anhand von Mäusen hat das Unternehmen gezeigt, dass eine Veränderung des PMS1-Spiegels sicher zu sein scheint und nicht mit Krebs in Verbindung gebracht wird. Rgenta testete Tausende verschiedener Chemikalien, von denen bekannt ist, dass sie die RNA-Konzentrationen verändern, und untersuchte dann, welche davon am besten geeignet sind, die Konzentration von PMS1, ihrem Ziel, zu verändern. Echt cool!
Ihr Medikamentenmolekül, das auf PMS1 abzielt, ist ein so genannter “Spleißmodulator”. Es wirkt, indem es das PMS1-Botschaftsmolekül verändert, was zu einer geringeren Menge des PMS1-Proteins führt. Sie haben gezeigt, dass ihr Medikament in vielen verschiedenen Zell- und Tiermodellen wirkt. Anschließend testeten sie ihr auf PMS1 abzielendes Medikament in HD-Zellen, die in einer Schale gezüchtet wurden. Theoretisch sollte die Senkung von PMS1 die somatische Expansion verringern. Und genau das haben sie auch gefunden! Durch die Senkung von PMS1 um etwa 90 % wurde die somatische Ausbreitung im Wesentlichen gestoppt.
Der Wirkstoff von Rgenta scheint auch nur auf den PMS1-Spiegel einzuwirken, ohne andere Proteine zu beeinträchtigen. Die von Rgenta vorgelegten Daten deuten darauf hin, dass der Wirkstoff in Tiermodellen gut funktioniert und gut ins Gehirn eindringt. Derzeit verfügt Rgenta nur über Daten, die zeigen, dass die Senkung des PMS1-Spiegels die somatische Expansion von HD-Zellen in einer Schale reduziert. Aber das Unternehmen verfolgt diesen Ansatz weiter und plant, sein Medikament in anderen HD-Modellen zu testen. Dies ist jedoch eine aufregende Neuigkeit, denn es bedeutet, dass ein weiteres vielversprechendes Medikament in der Pipeline ist, das eines Tages in die Klinik gelangen könnte, wenn die Tierstudien weiterhin so gut verlaufen.
Wir sind sehr froh, Tag 1 zu beenden, nachdem wir über so viele tolle Dinge berichtet haben, die in den Labors von Universitäten und Unternehmen auf der ganzen Welt passieren! Bleiben Sie dran für Tag 2, der in Kürze folgt!


