
Die dritte Dimension: Minigehirne nutzen, um Veränderungen der Gehirnentwicklung bei HD zu verstehen
Forschende zeigen, dass stark verlängerte CAGs im HD-Gen frühe Entwicklungsveränderungen verursachen können, indem sie 3D-Gehirnmodelle, sogenannte Organoide, verwenden. Was haben sie herausgefunden?

Eine neue Veröffentlichung nutzte winzige 3D-Gehirnmodelle, die aus menschlichen Zellen erstellt wurden, um zu zeigen, dass die HD-verursachende Mutation zu frühen Veränderungen in der Gehirnentwicklung führen könnte. Es ist jedoch klar, dass HD-Patienten voll ausgereifte Gehirnzellen entwickeln können und auch tun, die in den meisten Fällen jahrzehntelang normal funktionieren. Lass uns diese Ergebnisse also in den Kontext setzen und untersuchen, was diese Entwicklungsveränderungen, die mithilfe menschlicher Zellen in einer Petrischale entdeckt wurden, für HD-Patienten bedeuten könnten.
Menschliche Gehirnzellen gewinnen, ohne Gehirnproben zu entnehmen
Obwohl HD einzigartig für den Menschen ist, besitzen die meisten Organismen eine Version des Gens, das mutiert ist, um HD zu verursachen – Huntingtin, oder kurz Htt. Eine Vielzahl von Organismen kann zur Erforschung von HD verwendet werden, und jedes Modell kann verschiedene Aspekte der Krankheitsweise aufzeigen. Wenn ein Wissenschaftler beispielsweise wissen möchte, ob eine experimentelle Behandlung bei HD von Nutzen sein könnte, könnte er Fruchtfliegen oder sogar Würmer verwenden, um diese Antworten zu erhalten.

Obwohl Fliegen und Würmer sich stark von Menschen unterscheiden, haben sie eine sehr kurze Lebensdauer (etwa 14 Tage bei Fruchtfliegen), sodass Wissenschaftler schnell Antworten erhalten können. Wenn sie wissen wollen, was in einem komplexeren Gehirn passiert, wählen Wissenschaftler oft Mäuse. Um jedoch die Auswirkungen ihrer Arbeit auf den Menschen zu verstehen, müssen Wissenschaftler ihre Ideen am Menschen – oder zumindest an menschlichen Zellen – testen.
Im Jahr 2006 zeigten zwei unabhängige Wissenschaftler, dass man die biologische Zeitlinie einer Hautzelle umkehren kann, indem man sie darauf vorbereitet, sich in jeden anderen Zelltyp des Körpers zu verwandeln. In jüngerer Zeit wurden sogar Blutzellen verwendet. Diese vorbereiteten Zellen werden „induzierte pluripotente Stammzellen“ oder iPS-Zellen genannt.
Wenn Wissenschaftler daran interessiert sind, eine Gehirnerkrankung wie HD zu erforschen, können sie diese iPS-Zellen dann in die interessierenden Zelltypen, wie Neuronen, umwandeln. Und noch besser: Wenn die Haut- oder Blutzellen von einem HD-Patienten stammen, haben Wissenschaftler alles, was sie brauchen, um die Neuronen dieses Patienten zu untersuchen, ohne eine Gehirnprobe entnehmen zu müssen. Nicht nur super coole Wissenschaft, sondern auch eine großartige Nachricht für HD-Patienten, die ihre Gehirne gerne behalten möchten!
Normalerweise werden Zellen auf der flachen Oberfläche einer Petrischale gezüchtet, aber kürzlich haben Forschende einen Weg gefunden, iPS-Zellen dazu zu bringen, zu dreidimensionalen Zellkugeln heranzuwachsen – die einem kleinen Gehirn in einem frühen Entwicklungsstadium ähneln. Diese 3D-Strukturen werden Gehirnorganoide genannt und ähneln einem winzigen Gehirnmodell.
Das Züchten dieser Zellen in 3D ermöglicht es Forschenden, die Art und Weise zu untersuchen, wie sie sich organisieren, während der Organoid wächst, und liefert Informationen über sehr frühe Entwicklungsereignisse im Gehirn. Doch obwohl diese winzigen gehirnähnlichen Strukturen ähnliche frühe Entwicklungsmuster wie ein menschliches Gehirn aufweisen, sind sie keine funktionierende Replik und besitzen nicht die Fähigkeit zur kognitiven Funktion.
Du bist eine wunderschöne und einzigartige Schneeflocke
„In einer aktuellen Studie wurden diese Gehirnorganoide verwendet, um den Einfluss der HD-verursachenden Mutation auf ihre Entwicklung zu untersuchen. Dies geschah unter Verwendung von 4 verschiedenen Zelllinien, die in jeder Hinsicht identisch sind, bis auf eine: das HTT-Gen.“
In einer aktuellen Studie wurden diese Gehirnorganoide verwendet, um den Einfluss der HD-verursachenden Mutation auf ihre Entwicklung zu untersuchen. Dies geschah unter Verwendung von 4 verschiedenen Zelllinien, die in jeder Hinsicht identisch sind, bis auf eine: das HD-Gen. Aber Moment mal. Wie können 4 verschiedene Zelllinien identisch und doch unterschiedlich sein?
Man kann Menschen als Schneeflocken betrachten – wir sind alle auf unsere eigene Weise einzigartig, nicht nur mit offensichtlichen körperlichen Unterschieden, wie unterschiedlicher Haarfarbe oder Augenform, sondern auch auf genetischer Ebene. Jeder Mensch hat eine leicht einzigartige Zusammensetzung im Code seiner DNA, die ihn anders macht. Während also zwei Menschen den genetischen Code für Hände haben mögen, kann der eine sehr lange Finger haben und der andere kurze Finger.
Wenn Forschende Zellen von 2 Personen entnehmen, einer mit HD und einer ohne, enthalten ihre Zellen nicht nur die unterschiedlichen CAG-Längen des HTT-Gens dieser Person, sondern auch alle anderen genetischen Unterschiede, die sie einzigartig machen! Dies kann die Ergebnisse jedoch etwas verfälschen, da Forschende nicht wissen werden, ob gemessene Veränderungen auf Unterschiede im HD-Gen oder auf eine andere einzigartige Veränderung in der DNA dieser Person zurückzuführen sind.
Zurück zu diesen identisch unterschiedlichen Zellen – um Verwirrung in ihrer Studie darüber zu vermeiden, ob die Ergebnisse auf unterschiedliche CAG-Längen im HD-Gen oder auf einen anderen einzigartigen DNA-Code einer Person zurückzuführen sind, verwendeten Forschende eine Reihe von Zelllinien, die aus einer einzigen Zelllinie stammen, die nur innerhalb des HTT-Gens genetisch verändert wurde, sodass sie CAG-Repeats unterschiedlicher Größe enthält.
In diesem Fall wurde der CAG-Repeat-Trakt von 30 (um eine Person ohne HD-Risiko darzustellen) auf 45, 65 oder 81 (entsprechend HD-Beginn im Erwachsenenalter, Jugendalter oder Kindesalter) erhöht, während alle anderen Gene in diesen Zellen identisch blieben. So können die Forschenden nun sicher sein, dass alle Unterschiede, die sie zwischen diesen Zelllinien beobachten, explizit auf die von ihnen im HD-Gen induzierten Veränderungen zurückzuführen sind. Ziemlich clever!
Früh einsetzende juvenile HD ist möglicherweise keine rein degenerative Erkrankung
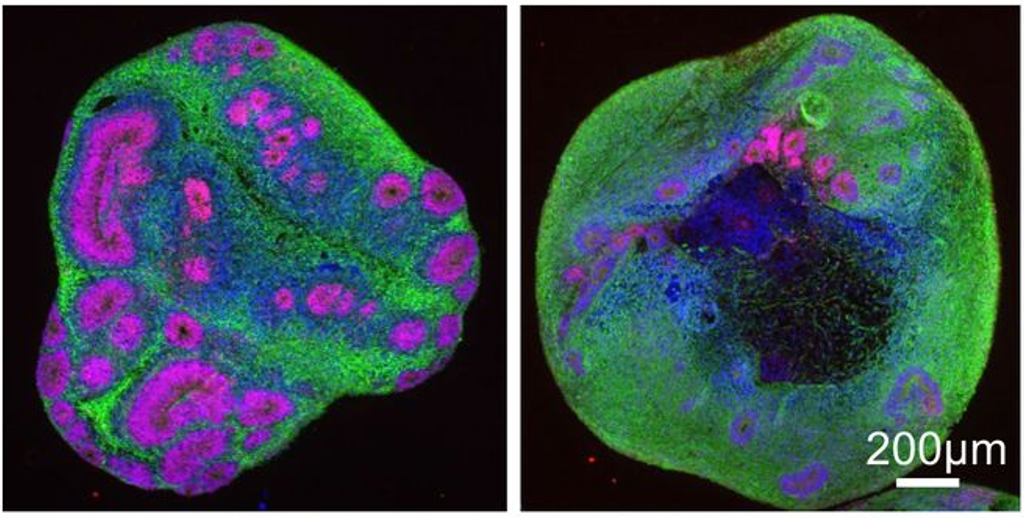
Als alle 4 Zelllinien zur Herstellung von Organoiden verwendet wurden, bemerkten die Forschenden als Erstes, dass, obwohl Organoide aus allen 4 Linien die gleiche Größe hatten, die HD-Organoide kleinere interne Strukturen entwickelten, die entwicklungsbedingt zur Bildung wichtiger Gehirnzellen, den Neuronen, führen, was darauf hindeutet, dass die Gehirnentwicklung gehemmt ist. Dies wurde jedoch nur bei Organoiden beobachtet, die dem HD-Beginn im Jugendalter (CAG von 65) und Kindesalter (CAG von 81) entsprechen, während die Organoide, die den HD-Beginn im Erwachsenenalter (CAG von 45) repräsentieren, den Organoiden ähnelten, die eine Person ohne HD repräsentieren.
Was bedeutet das also? Die Autoren interpretierten ihre Ergebnisse so, dass die HD-verursachende Mutation, insbesondere bei juvenilem Beginn, die Gehirnentwicklung hemmt. Eine alternative Idee ist jedoch, dass die HD-verursachende Mutation die Entwicklung lediglich verzögern könnte.
Um dies zu testen, untersuchten die Autoren ältere Organoide – sie maßen den Unterschied zwischen den Organoiden mit 30 und 81 CAGs und fanden heraus, dass diese selbst zu diesem späteren Zeitpunkt noch kleinere interne Strukturen aufwiesen. Es scheint also, dass, zumindest bei Fällen von juvenilem HD-Beginn, die Gehirnentwicklung in diesen Organoiden nicht nur verzögert, sondern eher zum Stillstand gekommen ist. Die Organoide mit Beginn im Jugend- und Erwachsenenalter wurden jedoch in diesem spezifischen Experiment nicht berücksichtigt.
Ein weiteres wichtiges Ergebnis dieser Studie deutet darauf hin, dass die Organoide mit juvenilem Beginn schneller zu Neuronen heranwachsen als die Organoide ohne die HD-Mutation. Doch wenn du auf dem Laufenden bist, was die HD-Organoid-Literatur angeht, mag dies etwas verwirrend erscheinen, denn eine vor etwa einem Jahr erschienene Arbeit fand genau das Gegenteil – dass aus iPS-Zellen stammende HD-Organoide langsamer zu Neuronen heranwachsen als Organoide ohne HD.
Bedeutet das also, dass eine Studie richtig und die andere falsch ist? Nein. Obwohl die beiden Studien gegensätzliche Effekte bei der Geschwindigkeit der HD-Organoid-Neuroentwicklung fanden, wurde jede Studie etwas anders durchgeführt, unter Verwendung unterschiedlicher Zelllinien und Messung der Effekte zu unterschiedlichen Zeitpunkten.
Worin sich beide Studien einig sind, ist, dass die HD-verursachende Mutation zu frühen Veränderungen in der Neuroentwicklung führt. Doch nur weil Ergebnisse auf frühe Entwicklungsveränderungen hindeuten, bedeutet das nicht, dass diese Veränderungen nicht kompensiert werden können. Tatsächlich identifizierten die Autoren der jüngeren Studie ein Medikament, das die Fähigkeit besitzt, die geringeren Messwerte, die sie in den Organoiden mit juvenilem HD-Beginn beobachteten, teilweise wiederherzustellen!
„Worin sich beide Studien einig sind, ist, dass die HD-verursachende Mutation zu frühen Veränderungen in der Neuroentwicklung führt. Doch nur weil Ergebnisse auf frühe Entwicklungsveränderungen hindeuten, bedeutet das nicht, dass diese Veränderungen nicht kompensiert werden können.“
Aber was ist mit den Organoiden, die den Beginn der HD im Jugend- und Erwachsenenalter repräsentieren? Wenn du ein Detailfanatiker bist, hast du vielleicht bemerkt, dass sich die meisten Ergebnisse dieser Studie nur auf Organoide konzentrieren, die den juvenilen HD-Beginn repräsentieren, was etwa 5–10 % der HD-Patientenpopulation ausmacht. Das bedeutet, dass diese Experimente eine seltene Form einer bereits seltenen Krankheit untersuchen. Die Autoren dieser Studie sind jedoch sorgfältig bei der Interpretation ihrer Ergebnisse im Kontext dessen, was ihre Daten repräsentieren, und sagen: „Insgesamt deuten diese Ergebnisse darauf hin, dass HD, zumindest in ihren früh einsetzenden juvenilen Formen, möglicherweise keine rein neurodegenerative Erkrankung ist und dass eine abnormale Neuroentwicklung ein Bestandteil ihrer Pathophysiologie sein könnte.“
Brandaktuell
Eine Sache, die bei dieser Studie zu beachten ist, ist, dass sie derzeit in einem Repository namens BioRxiv (ausgesprochen „Bio-Archiv“) veröffentlicht ist. BioRxiv ist eine phänomenale Ressource, da es Daten vor dem Druck veröffentlicht und für jedermann zugänglich macht. Obwohl dies Daten schneller an die breite Masse bringt, bedeutet es auch, dass sie den wissenschaftlichen Prozess der „Peer-Review“ noch nicht durchlaufen hat, einer unvoreingenommenen Bewertung der Arbeit durch andere Wissenschaftler auf diesem Gebiet, die nicht mit dem Projekt verbunden sind.
Die Peer-Review ist entscheidend, um die Strenge wissenschaftlicher Studien aufrechtzuerhalten, und bietet den Autoren der Arbeit eine durchdachte externe Perspektive von anderen Experten auf ihrem Gebiet. Da diese Studie noch keiner Peer-Review unterzogen wurde, könnten Gutachter vor der Veröffentlichung zusätzliche Arbeiten anfordern, um einige der Ergebnisse zu klären, oder sogar eine weitere Untersuchung der Organoide verlangen, die den Beginn der HD im Jugend- und Erwachsenenalter repräsentieren. Man kann diese Studie also im Moment wie ein unfertiges Buch betrachten – wir müssen nach ihrer endgültigen Veröffentlichung wieder reinschauen, um die ganze Geschichte zu erfahren.
Normalisieren sich diese Entwicklungsveränderungen jemals?
Obwohl die Organoide sehr cool sind, weil sie uns mithilfe menschlicher Zellen etwas über HD-bedingte Veränderungen auf zellulärer Ebene erzählen können, die früh in der Entwicklung auftreten, brauchen wir wirklich Daten von Patienten, um die Auswirkungen zu interpretieren, die etwaige Veränderungen auf einen voll entwickelten Menschen haben könnten oder auch nicht.

Eine andere Studie tat genau das und untersuchte die Größen verschiedener Gehirnstrukturen von Kindern und Jugendlichen (im Alter von 6 bis 18 Jahren) mit und ohne die im Erwachsenenalter einsetzende Form der HD-Mutation mittels MRT. Dies sind Kinder ohne HD-Symptome, deren Eltern zugestimmt haben, dass sie an der Forschung teilnehmen, um die frühesten Veränderungen, die durch die HD-Mutation verursacht werden, besser zu verstehen.
Diese Studie berichtete über ein größeres Striatum (eine der primären Gehirnregionen, die von der HD-verursachenden Mutation betroffen sind) bei HD-Mutation tragenden Kindern frühzeitig, im Alter von 6 bis 11 Jahren, während HD-Gen-negative Kinder später, im Alter von 11 bis 18 Jahren, ein größeres Striatum aufweisen. Es scheint also, dass die Gen-positiven Kinder eine schnellere Neuroentwicklung haben, zumindest des Striatums, aber dass Gen-negative Kinder schließlich aufholen und in den in dieser Studie untersuchten Altersgruppen ein größeres Striatum aufweisen. Dieser Unterschied scheint jedoch recht gering zu sein, mit nur etwa 1 ml Schwankung – etwa ¼ eines Gummibärchens zur Veranschaulichung.
Studien wie diese, die nicht-invasive Methoden verwenden, die sehr kleine Veränderungen erkennen können, sind genau das, was benötigt wird, um den Beitrag von HD zur Gehirnentwicklung zu bewerten. Sie werden helfen, Ergebnisse aus Studien, die eine sehr frühe Entwicklung repräsentieren, wie die Organoid-Studie in einer Petrischale, im Kontext menschlicher Patienten zu interpretieren.
Letztendlich ist die Forschung, die Gehirnentwicklungsveränderungen infolge von HD aufzeigt, neu, und obwohl biologisch interessant, wissen Forschende noch nicht, was das alles im Kontext der Krankheit bedeutet. Es ist jedoch wichtig zu bedenken, dass Forschende auch daran arbeiten, Mechanismen zu entdecken, die etwaige von ihnen berichtete Gehirnentwicklungsveränderungen kompensieren können.
Mehr erfahren
- Verlängerte Huntingtin-CAG-Repeats stören das Gleichgewicht zwischen neuronaler Vorläuferzell-Expansion und Differenzierung in menschlichen zerebralen Organoiden (Open Access)
- Fehlerhafte neuronale Determination und Zellpolarisation werden durch Modulation früher HD-Phänotypen rückgängig gemacht (vollständiger Artikel erfordert Bezahlung oder Abonnement)
- Abnormale Gehirnentwicklung bei Kindern und Jugendlichen, die mutiertes Huntingtin tragen (vollständiger Artikel erfordert Bezahlung oder Abonnement)
Quellen & Referenzen
Weitere Informationen zu unseren Offenlegungsrichtlinien finden Sie in unseren FAQ…


